gkt-horizontal-line
※このウェブページは中学校理科3年の学習内容です。<3年p.136>
探究3 結果から考察する
結果
図3 探究3の酸の結果例
塩酸や硫酸の場合は,青色リトマス紙の陰極側が赤色に変わった。
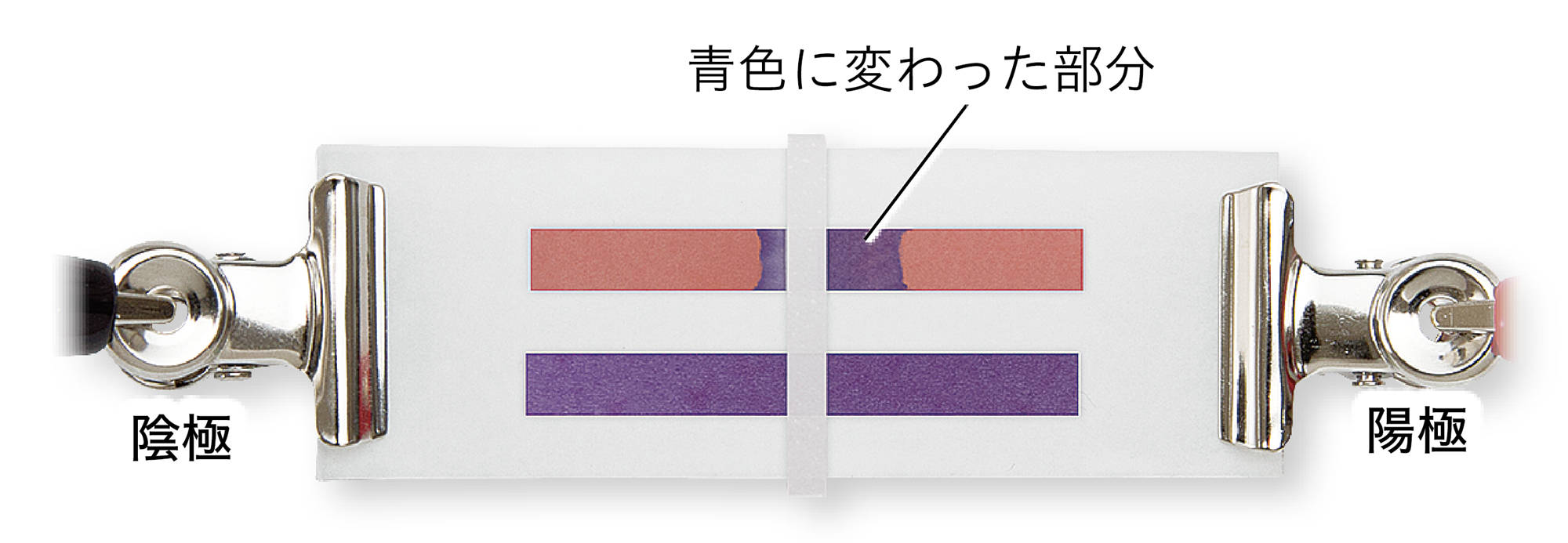
図4 探究3のアルカリの結果例
水酸化ナトリウム水溶液,水酸化カリウム水溶液の場合,赤色リトマス紙の陽極側が青色に変わった。
考察
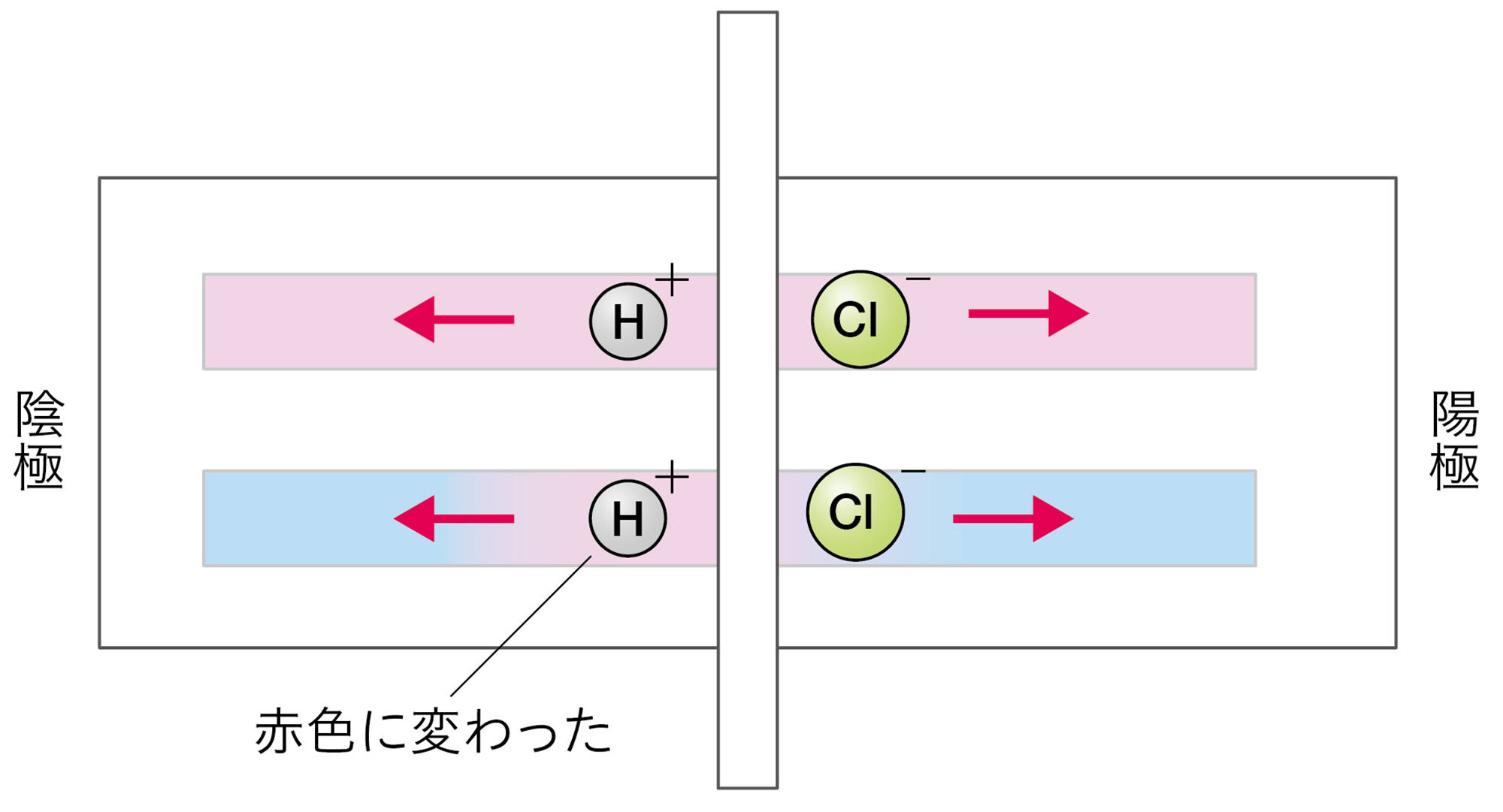
塩酸や硫酸に共通する陽イオンは,水素イオンである。リトマス紙の陰極側が赤色に変わったことから,水素イオンが陰極に引きつけられ,水素イオンがリトマス紙を赤色に変えたと考えることができる。
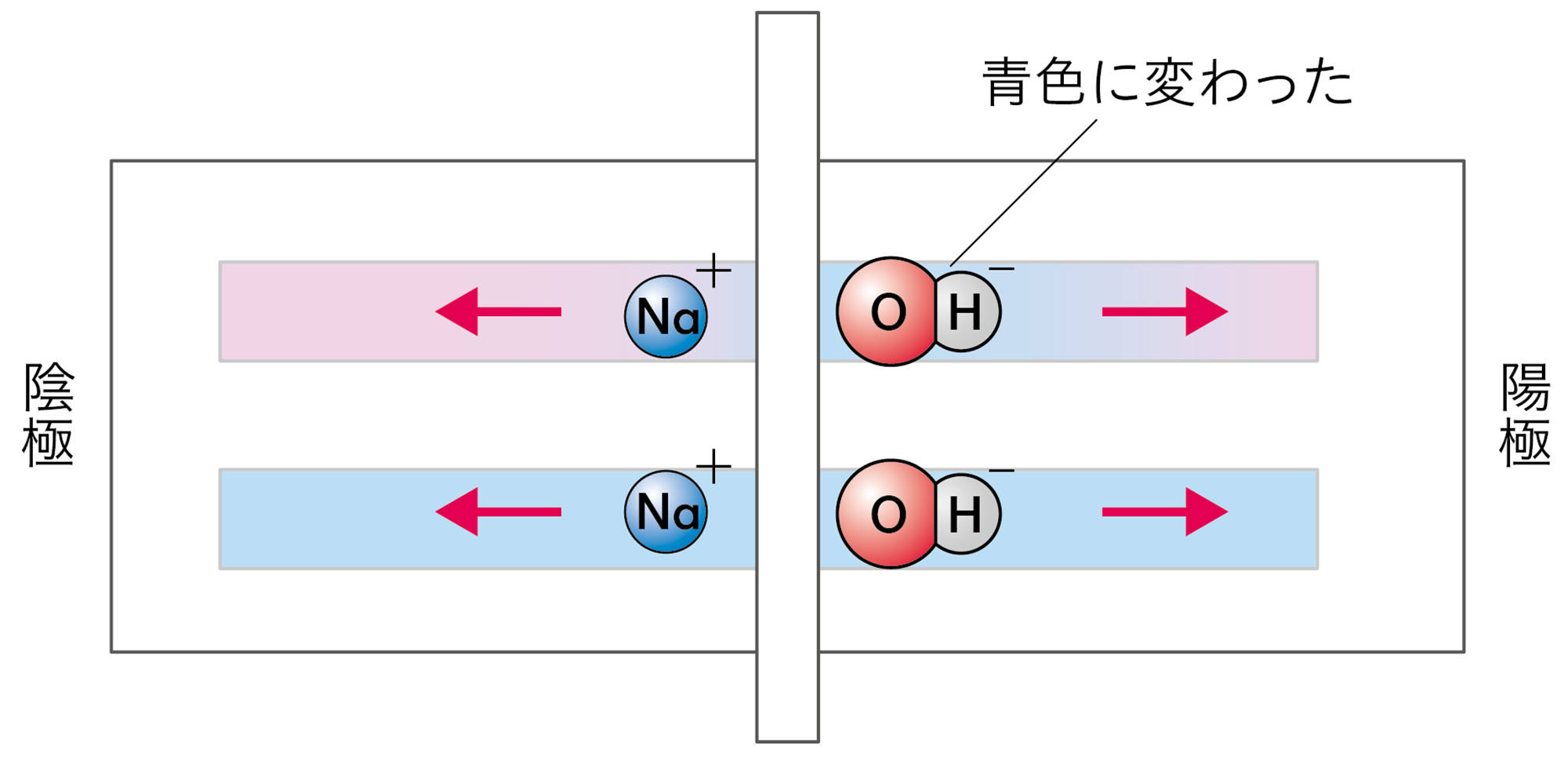
水酸化ナトリウム水溶液や水酸化カリウム水溶液に共通する陰イオンは,水酸化物イオンである。リトマス紙の陽極側が青色に変わったことから,水酸化物イオンが陽極に引きつけられ,水酸化物イオンがリトマス紙を青色に変えたと考えることができる。
○以上のことから,水素イオンが酸性の性質を示す正体で,水酸化物イオンがアルカリ性の性質を示す正体だと考えられる。
図5 探究3の結果を説明するモデル例
エタノール水溶液,砂糖水,硝酸カリウム水溶液の場合,同じ方法で実験しても変化はありませんでした。