gkt-horizontal-line
※このウェブページは中学校理科1年の学習内容です。<1年p.67>
2|溶解度と再結晶
1 飽和
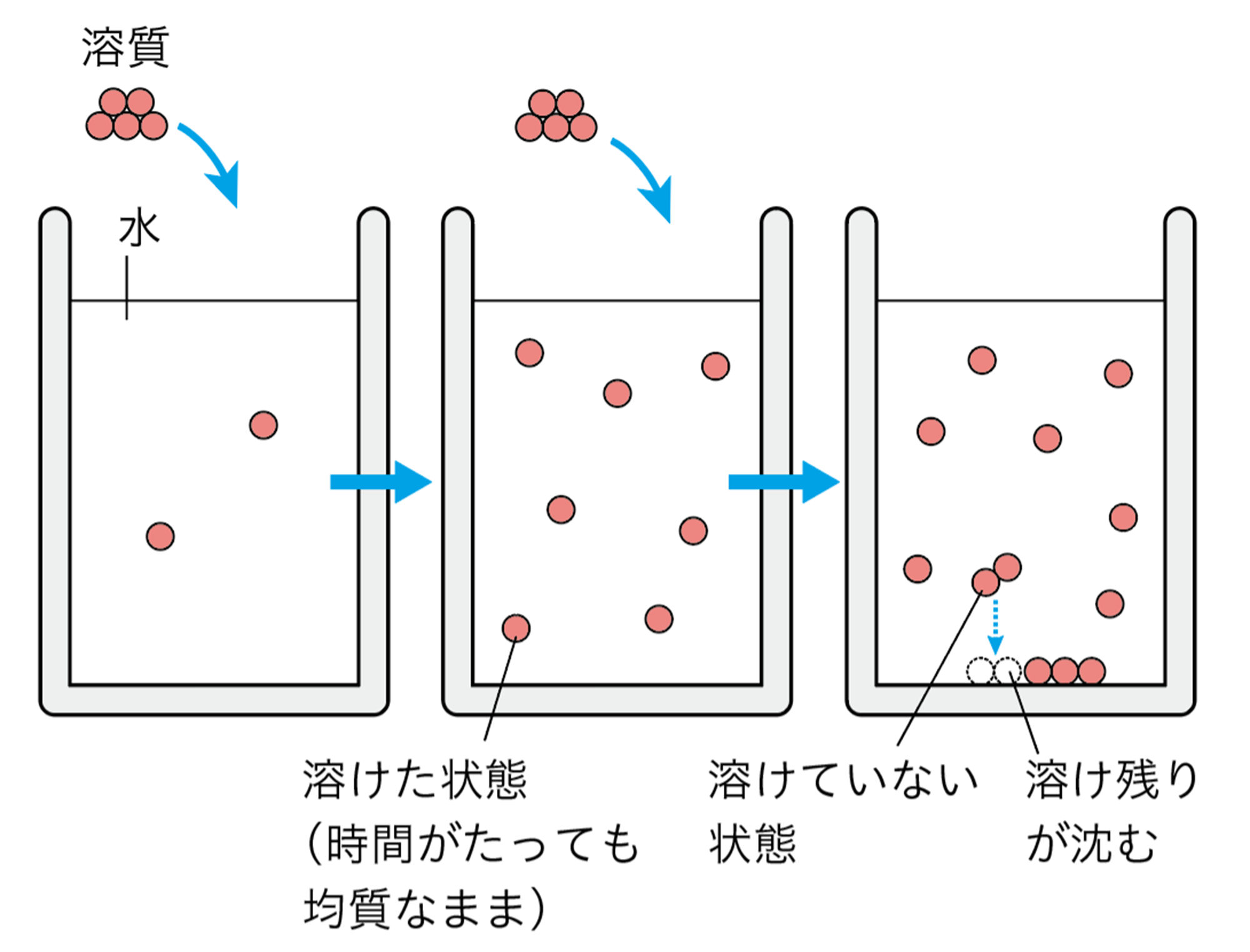
水に塩化ナトリウムを入れると,塩化ナトリウム水溶液ができる。しかし,塩化ナトリウムが多くなると,いくらかき混ぜても溶けきれずに,容器の底に残るようになる(図6)。溶質がそれ以上水に溶けきれなくなったときを飽和したといい,その水溶液を【飽和水溶液】という。
2 溶解度
一定の量の水に溶ける物質の質量は,物質によって決まっている。水100gに物質を溶かして飽和水溶液にしたとき,溶けた物質の質量を【溶解度】という。一般に,固体の物質の溶解度は,温度が高くなると大きくなるが,その度合いは物質によって異なっている。

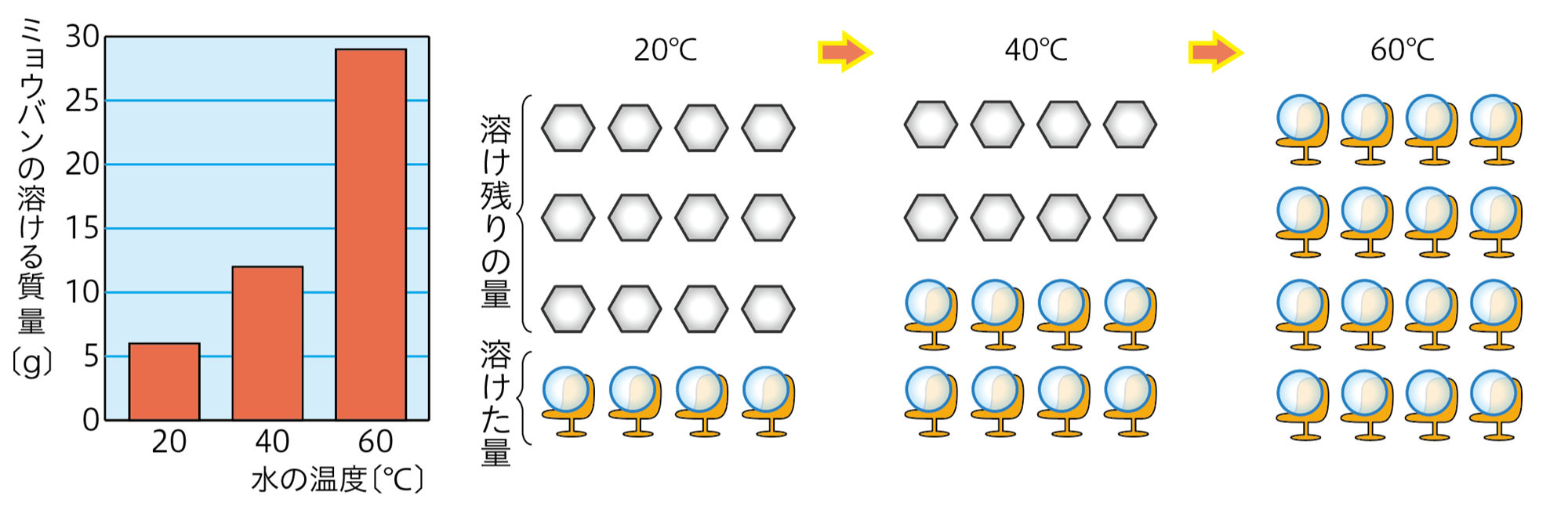
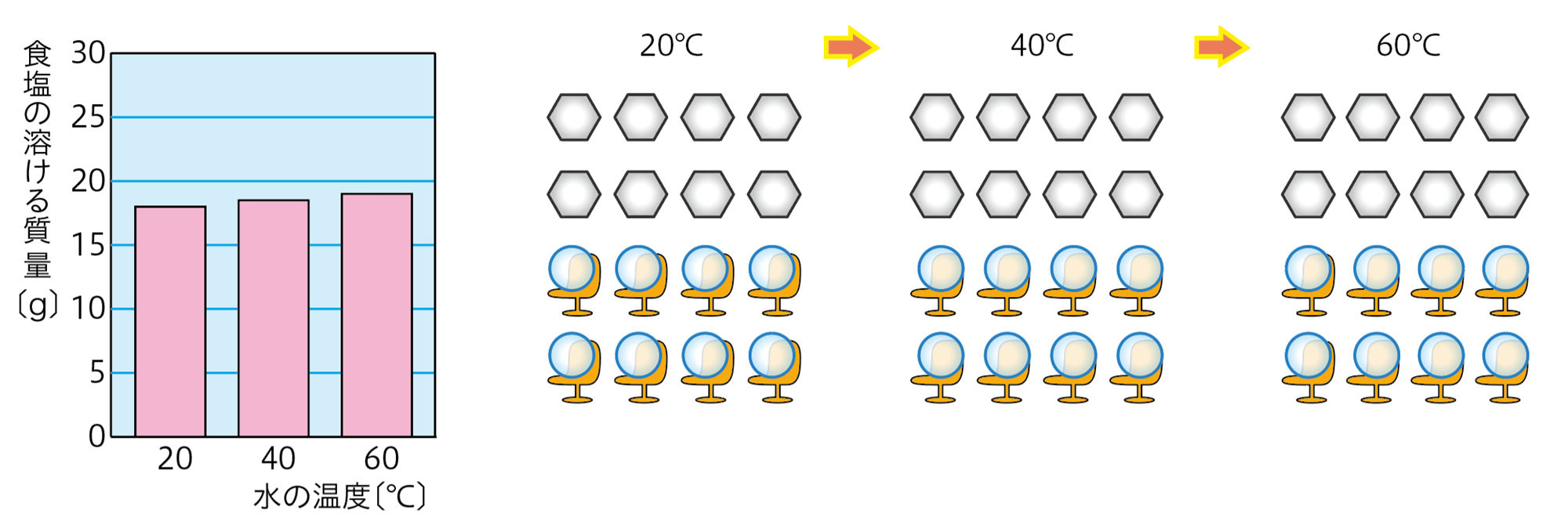
溶解度のちがいを「いす取りゲームのモデル」で考えてみましょう。
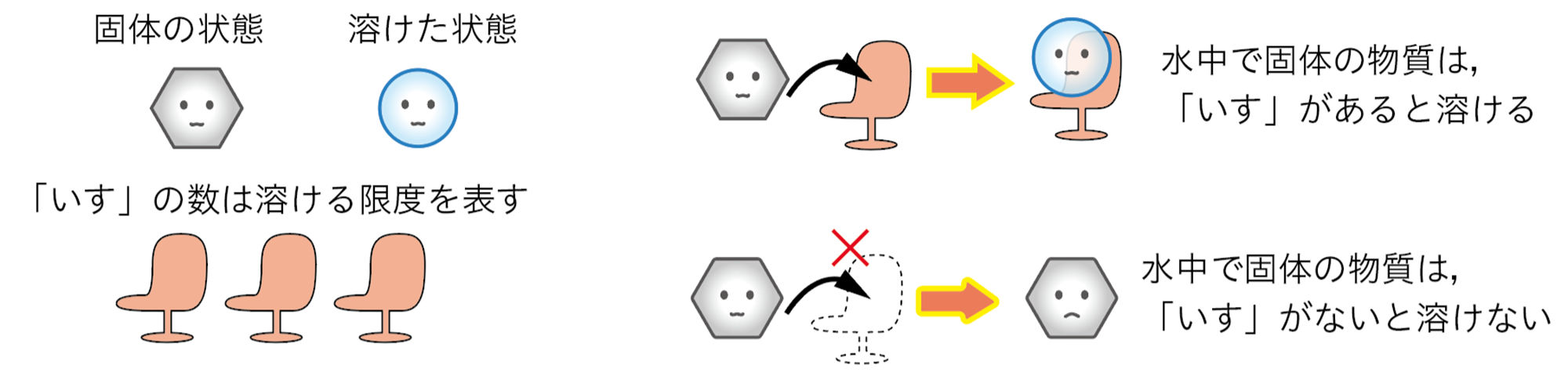
ミョウバンは,水温が高いほどたくさん溶けますね。これは,温度が上がるほど「いす」が増えると考えればいいんですね。


食塩のように,水温を上げてもあまり溶ける量が変わらない場合は,「いす」の数が変化しないと考えるんですね。