gkt-horizontal-line
※このウェブページは中学校理科2年の学習内容です。<2年p.59>
3 還元
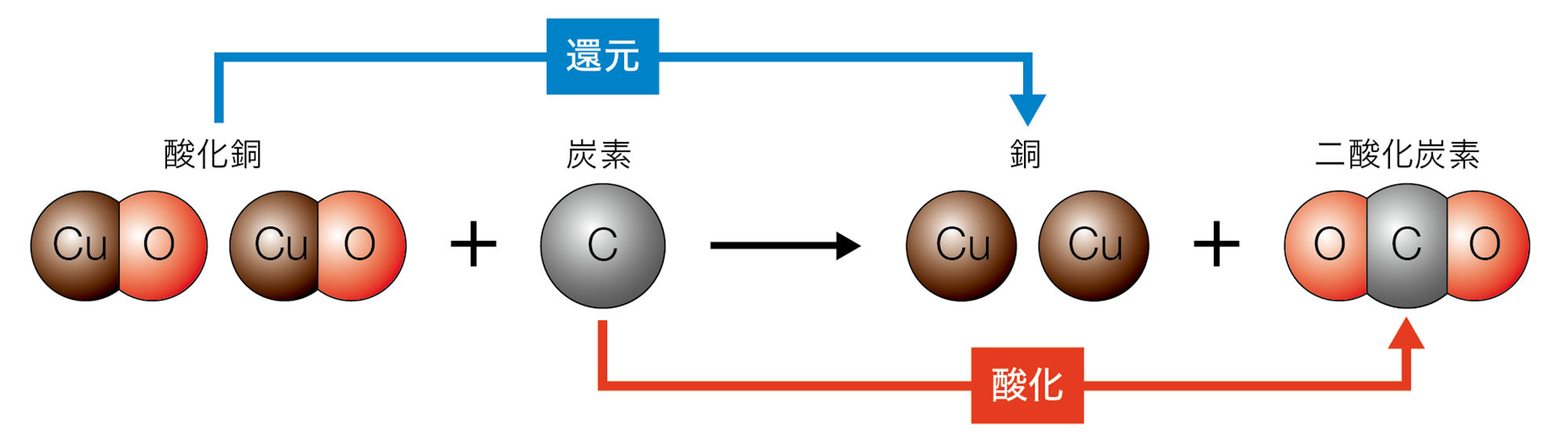
探究7のように,酸化物から酸素を取り除く化学変化を【還元】という。還元は,酸化と反対の化学変化である。酸化銅が還元されるとき,炭素は酸化銅から取り除いた酸素によって酸化されている。このように,還元が起こるときは,同時に酸化も起こる(図6)。
還元が起こるのは,酸素と結びつきやすい物質(探究7の場合は炭素)が,酸化銅の酸素と結びついて酸化物(二酸化炭素)となり,もとの酸化物(酸化銅)が単体(銅)として残るからである。
この実験から,炭素と銅を比べると炭素の方が酸素と結びつきやすいことがわかりますね。


酸化鉄の還元は実験しないのですか?
酸化鉄の還元には,とても高い温度が必要で,ガスバーナーでは火力が足りないのです。

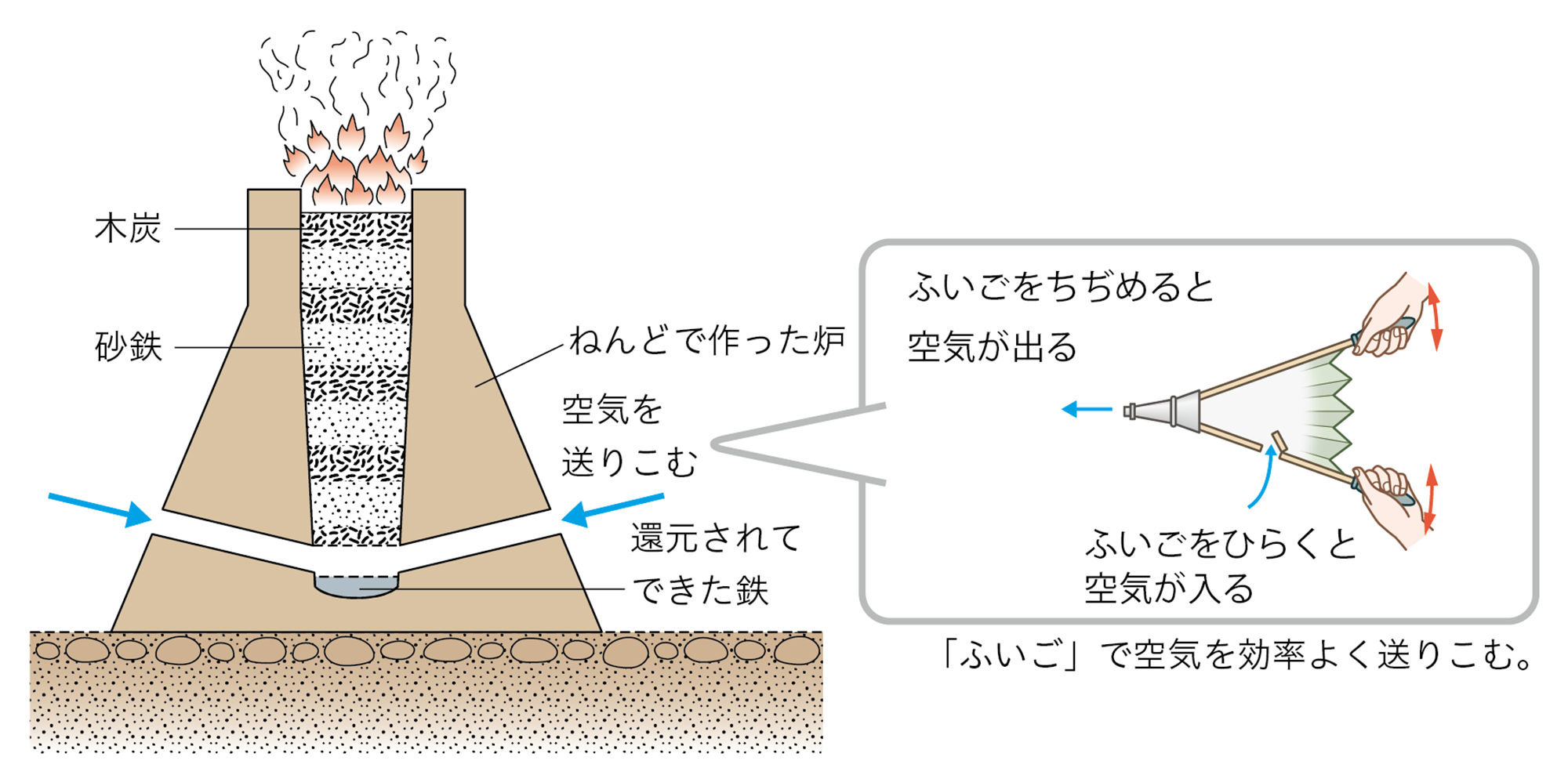
図7 還元の利用-たたら製鉄-