gkt-horizontal-line
※このウェブページは中学校理科2年の学習内容です。<2年p.61>
1 化学変化と熱
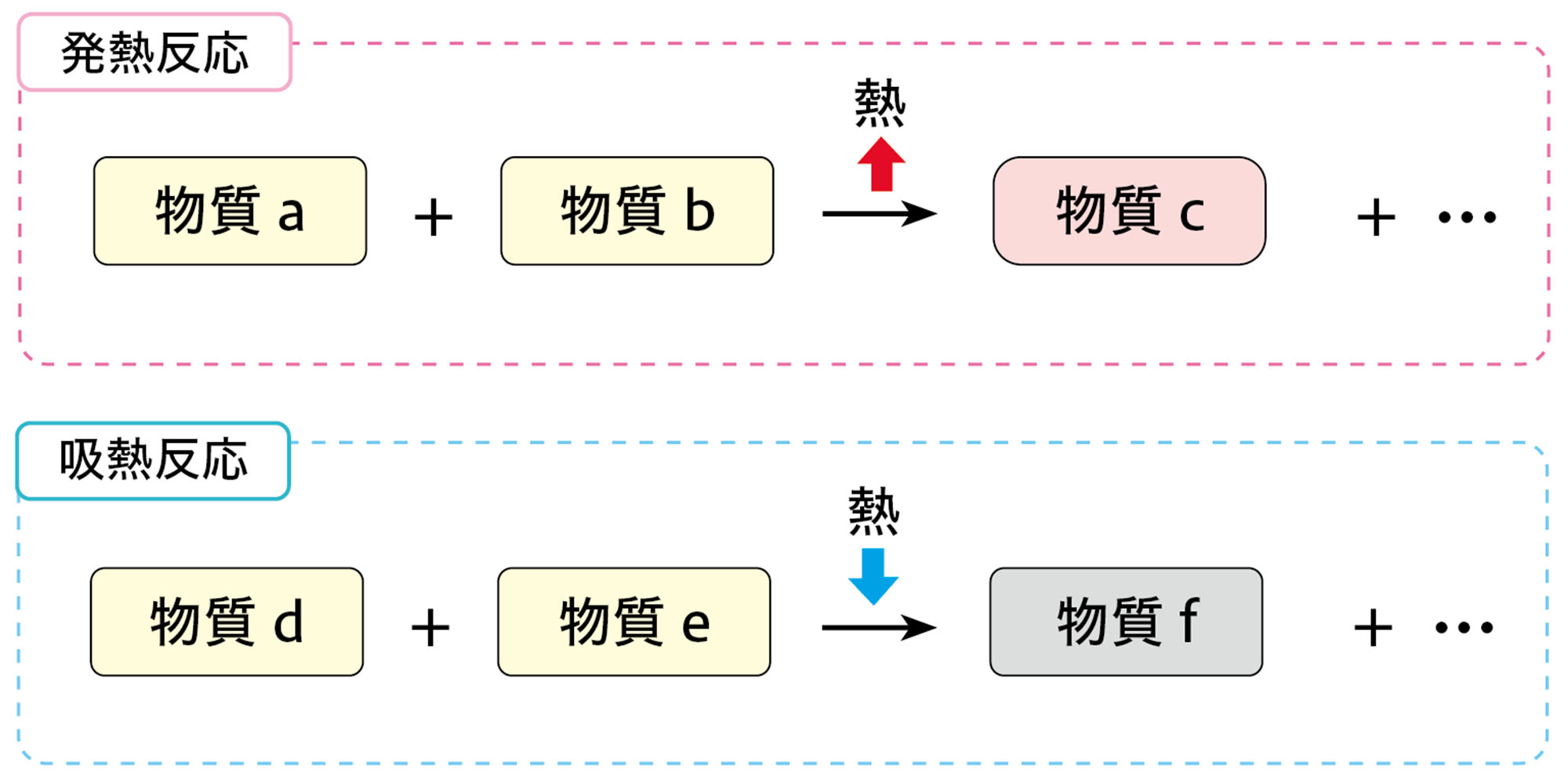
前ページの探究8では,化学変化が起こるときに熱の出入りをともなうことがわかる。このうち,温度が上がる反応を【発熱反応】という。温度が上がるのは,化学変化にともなって熱を外部に放出するからである。また,温度が下がる反応を【吸熱反応】という。温度が下がるのは化学変化をするために熱を必要とし,外部から熱を吸収するからである(図8)。
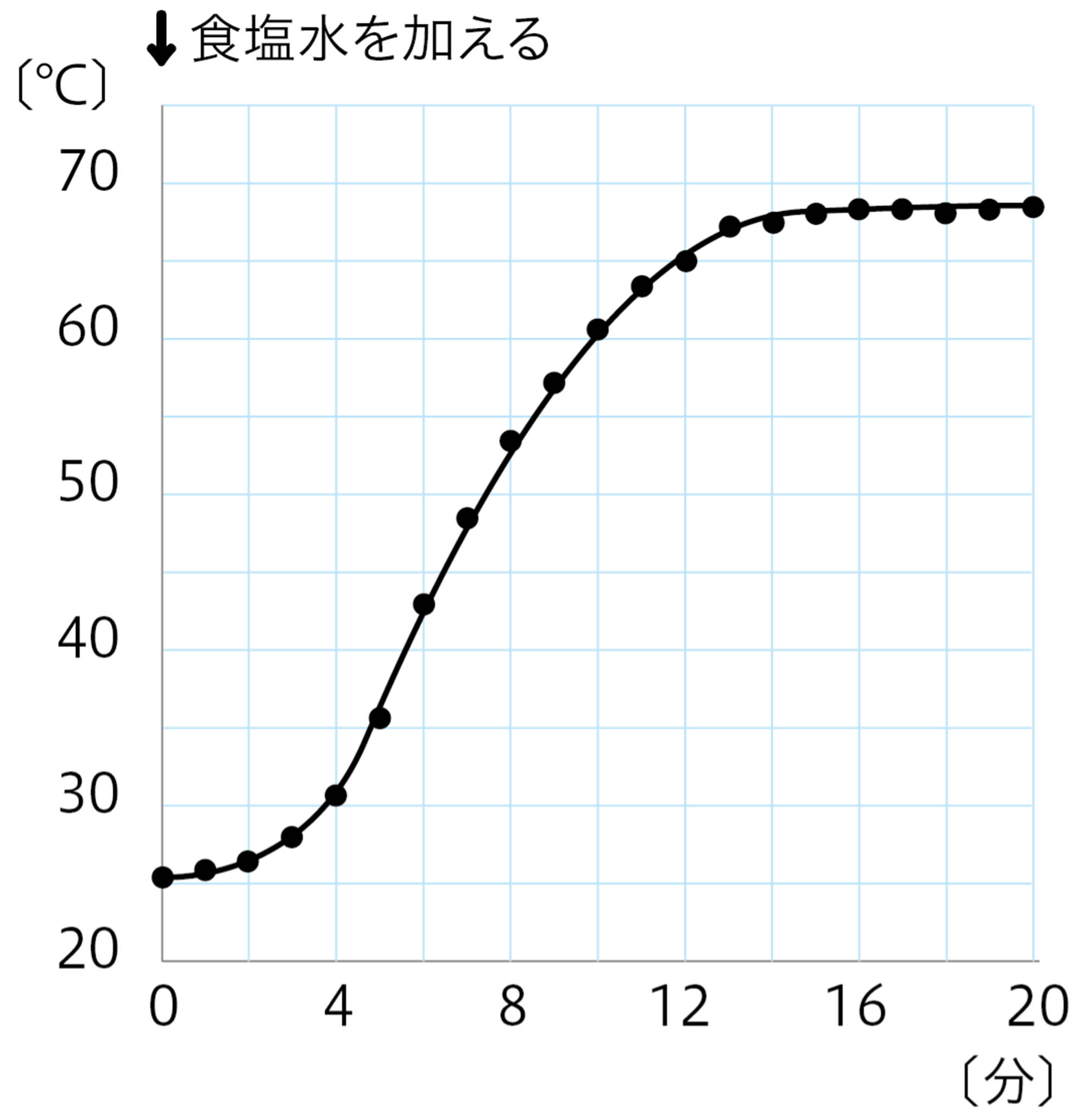
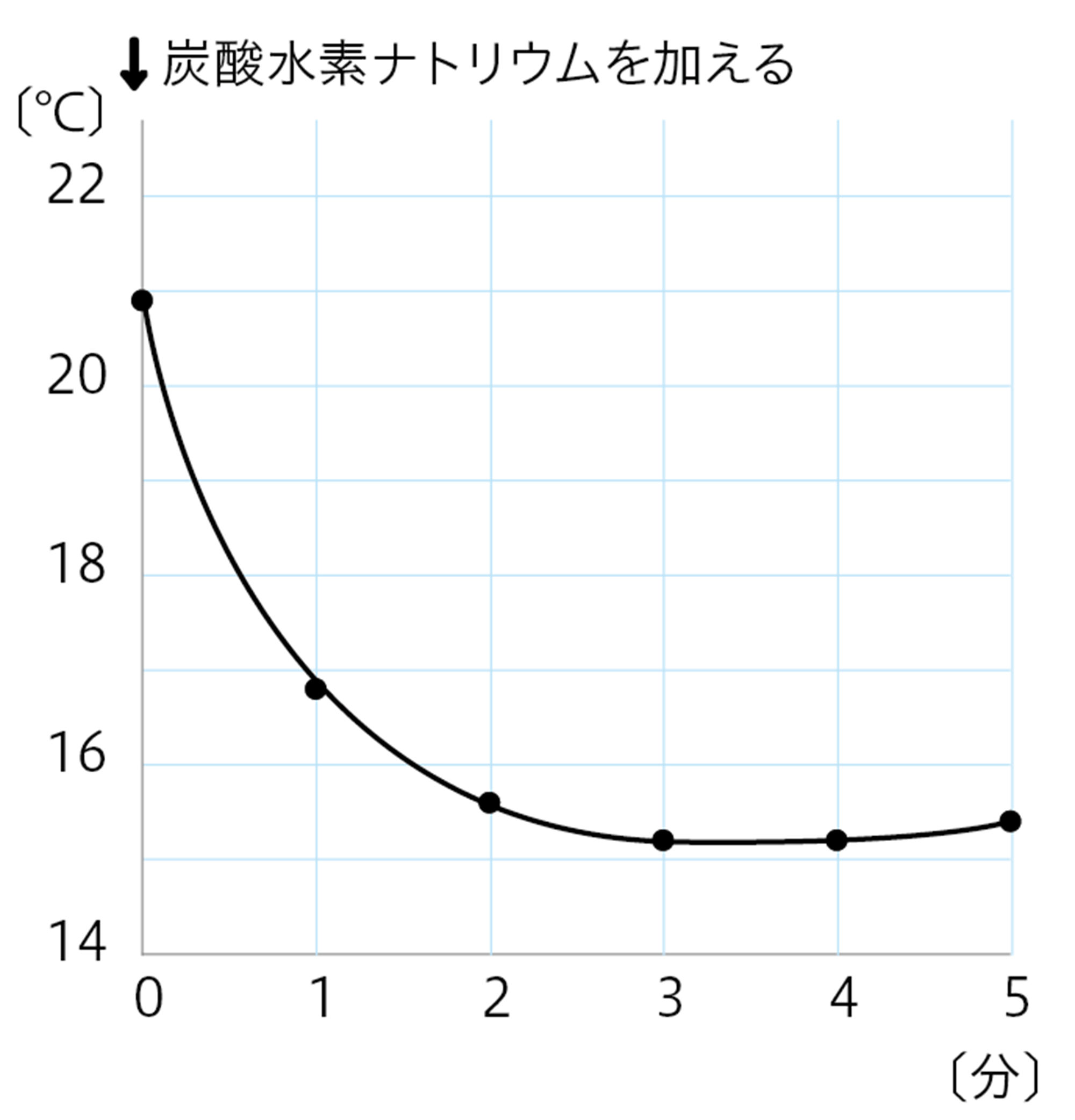
図9 探究8の結果例
図10 化学変化と熱の利用例
注意!! ここでは説明のために分解している。自分で分解してはいけない。