gkt-horizontal-line
※このウェブページは中学校理科3年の学習内容です。<3年p.143>
1 中和
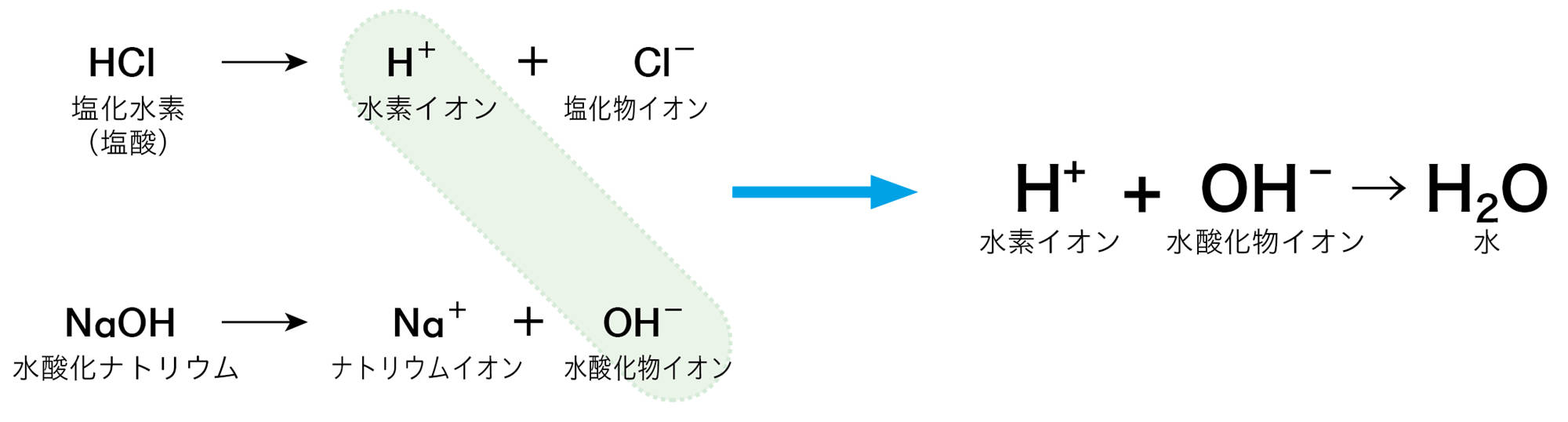
酸性の水溶液とアルカリ性の水溶液を混ぜると,たがいにその性質を打ち消し合う。このような化学変化を【中和】❶といい,このとき水ができる。中和は,酸の水素イオンH⁺とアルカリの水酸化物イオンH₂Oとが結びついて水HO⁻になる化学変化である(図14)。
水素イオンと水酸化物イオンは,もっている電気が異なるので,結びつくと電気を帯びていない状態になりますね。

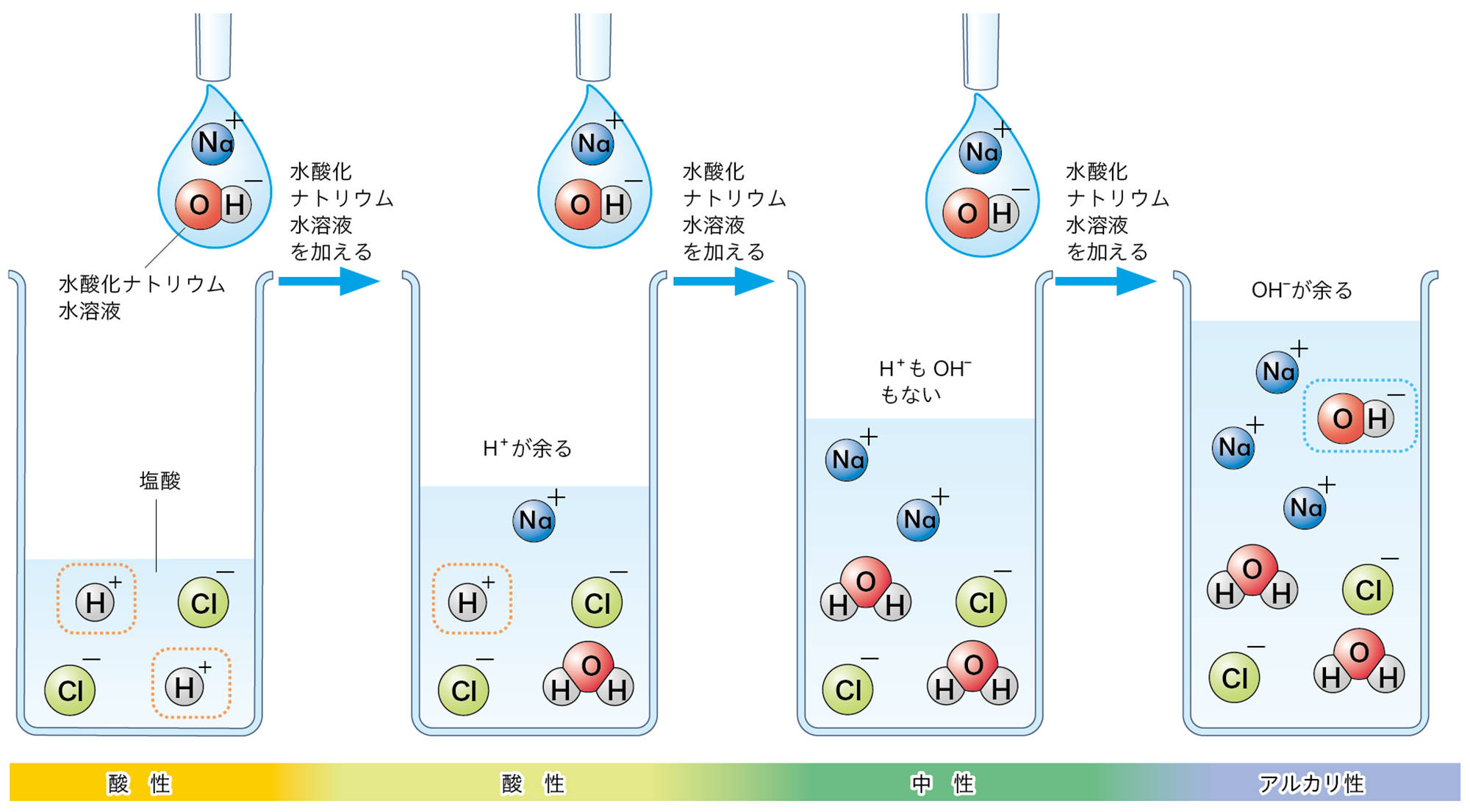
塩酸と水酸化ナトリウム水溶液を混ぜると中和が起こるが,混合液がいつも中性になるとは限らない。図15のように,水素イオンH⁺が余れば水溶液は酸性を示し,水酸化物イオンOH⁻が余れば水溶液はアルカリ性を示す。
中性にならなくても,中和は起こっていることに気をつけましょう。

❶ H⁺とOH⁻が同数で中和するとき,どちらも残らずに水ができて,酸性とアルカリ性が相互に完全に打ち消される。