※このウェブページは中学校理科2年の学習内容です。<2年p.10>
1|化学変化と原子
1 物質の変化
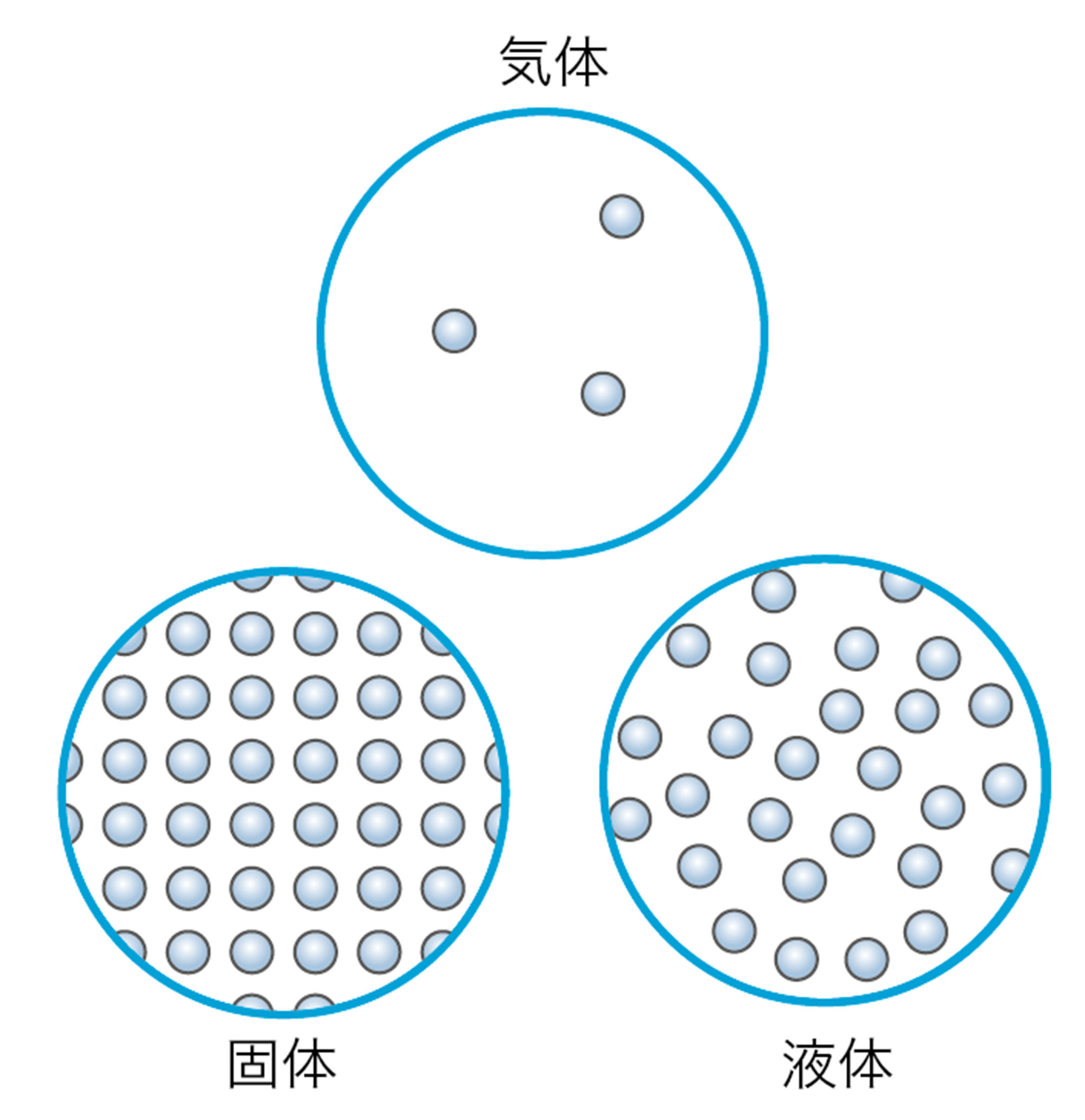
中学校1学年では,物質の性質を「粒子のモデル」で考えた。たとえば,ロウの粒子,エタノールの粒子,砂糖の粒子,酸素の粒子…というように,粒子のモデルは,物質の性質を説明するときのよい方法である。
ただし,この粒子のモデルでは,まだ説明できないこともある。たとえば,小学校から中学校1学年までの学習で,図2のような物質の変化をあつかってきた。これらの現象をみると,もとの物質とは異なる物質ができたり,もとの物質にはふくまれていなかった物質が現れたりしているように考えられる。
図2 有機物,無機物の加熱

これらの変化は,粒子のモデルでどのように説明できるでしょうか。
※このウェブページは中学校理科2年の学習内容です。<2年p.11>
物質そのものが変化するとき,粒子のモデルを使って,どのように科学的に探究できるだろうか。
探究1 物質そのものの変化

中学校1学年で,有機物,無機物を加熱する実験を行いました。
このとき,物質と酸素の間に何が起こっていたのでしょうか。図3では,木(有機物)と鉄(無機物)を加熱します。木を加熱したあと,質量は(a)のように減ります。では,鉄(b)はどのように変化するでしょうか。
物質が変化するようすを粒子のモデルでどのように表すことができるか。

物質が燃えるには,酸素が必要だよね。
物質が燃えるのは状態変化ではないよね。


「燃える」とは,炎が出たり赤く光ったりして,そのあとに黒くなることだと思う。このとき質量が減るんじゃないかな。

質量が減ったことを調べるためには,物質を加熱する前後で,質量を比べれば いいね。電子てんびんを使おうかな。
物質を加熱したあとは,黒くなってぼろぼろになるよね。加熱する前後での物質の性質のちがいを確かめるには,どうすればいいかな。

※このウェブページは中学校理科2年の学習内容です。<2年p.12>
準備
スチールウール(鉄),塩酸(5%),電子てんびん,ピンセット,ガラス管,ゴム管,アルミニウムはく,薬包紙,乾電池,豆電球,導線,試験管(2),試験管立て,加熱器具,スポイト,軍手,保護めがね
1.質量をはかる
スチールウール約8gをまるめて質量をはかる。
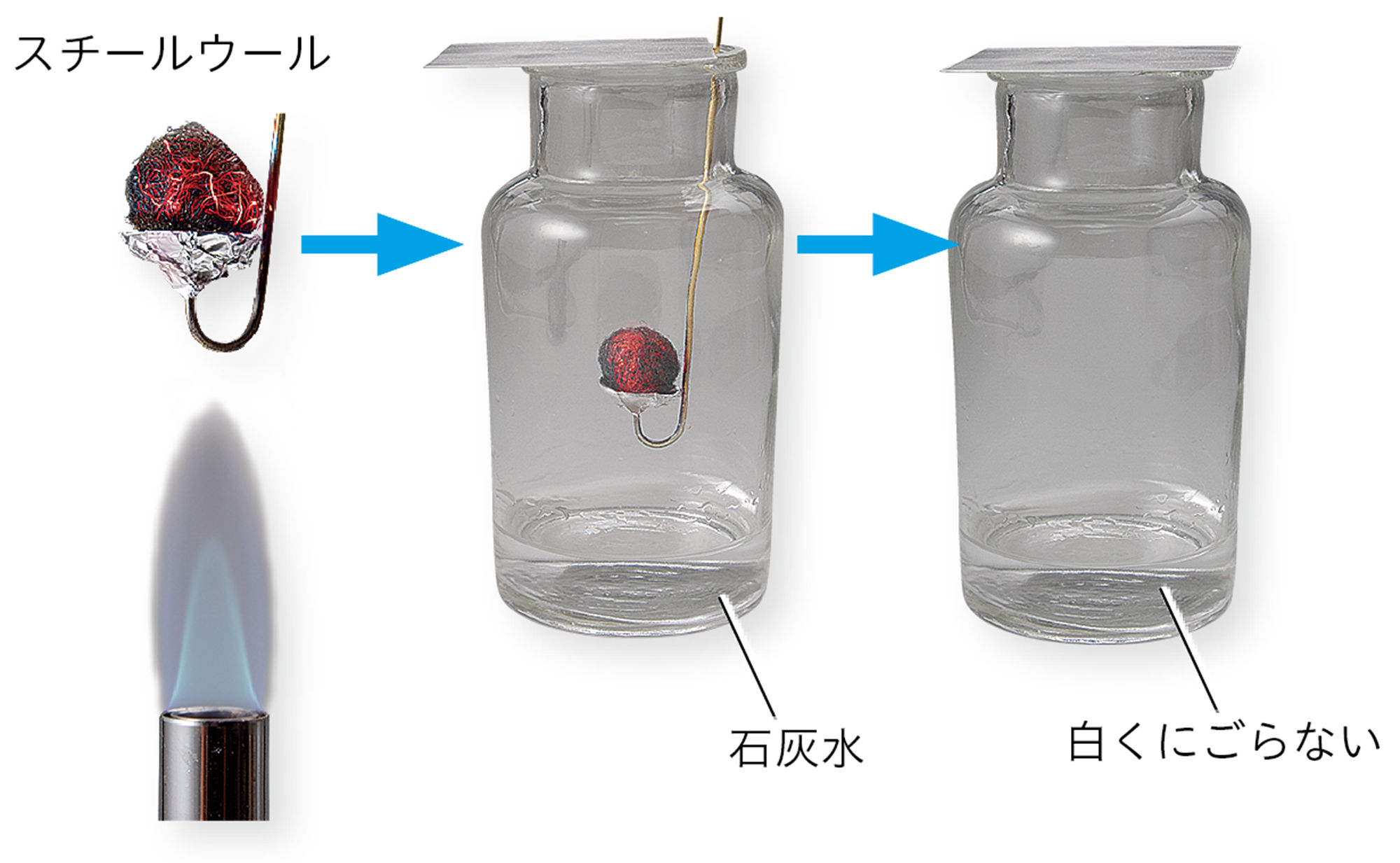
2.スチールウールを加熱する
燃えたスチールウールが飛び散るため,アルミニウムはくをしく。
ガスバーナーでスチールウールに火をつける。

はく息には,二酸化炭素が多いから,二酸化炭素をふきかけているのかな?
いいえ,息をふきかけるときに風が起きて,まわりの空気をまきこんで燃えているスチールウールに当たります。空気をふきかけていると考えましょう。

※このウェブページは中学校理科2年の学習内容です。<2年p.242>
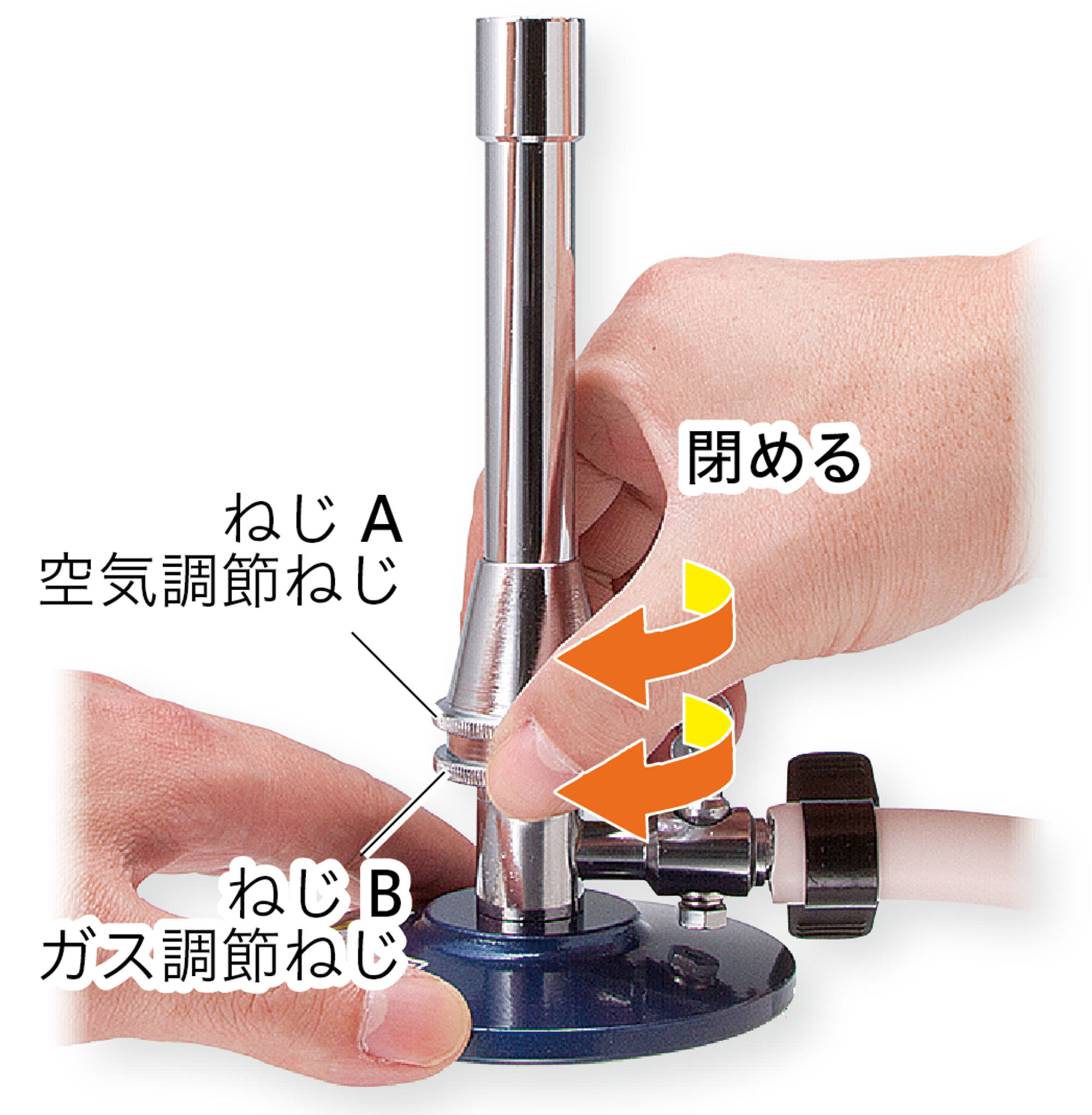
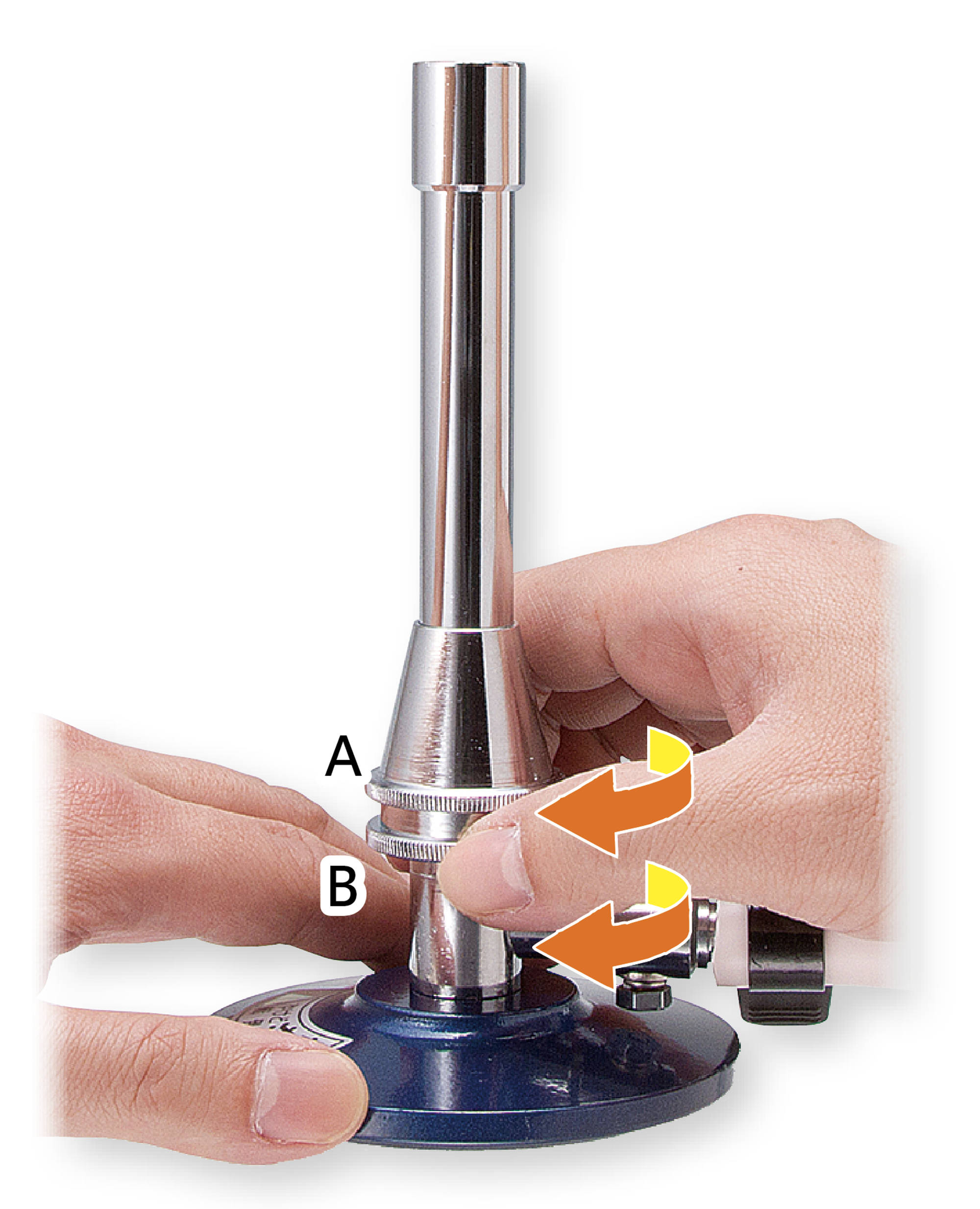
基本操作 ガスバーナーの使い方
注意!! 火を消した直後は,ガスバーナーの口の付近は熱くなっているので,さわらないよう注意する。
※このウェブページは中学校理科2年の学習内容です。<2年p.13>
3.加熱する前後の物質を調べる
ポイント
ポイント
- スチールウールは加熱する前後でどのように変化したか。
- スチールウールを加熱するときの変化を,粒子のモデルでどのように表すことができるか。

加熱済みのスチールウールは,次の探究で使用するので,とっておきます。
※このウェブページは中学校理科2年の学習内容です。<2年p.14>
探究1 結果から考察する
ここでは,結果と考察の例を示していきます。

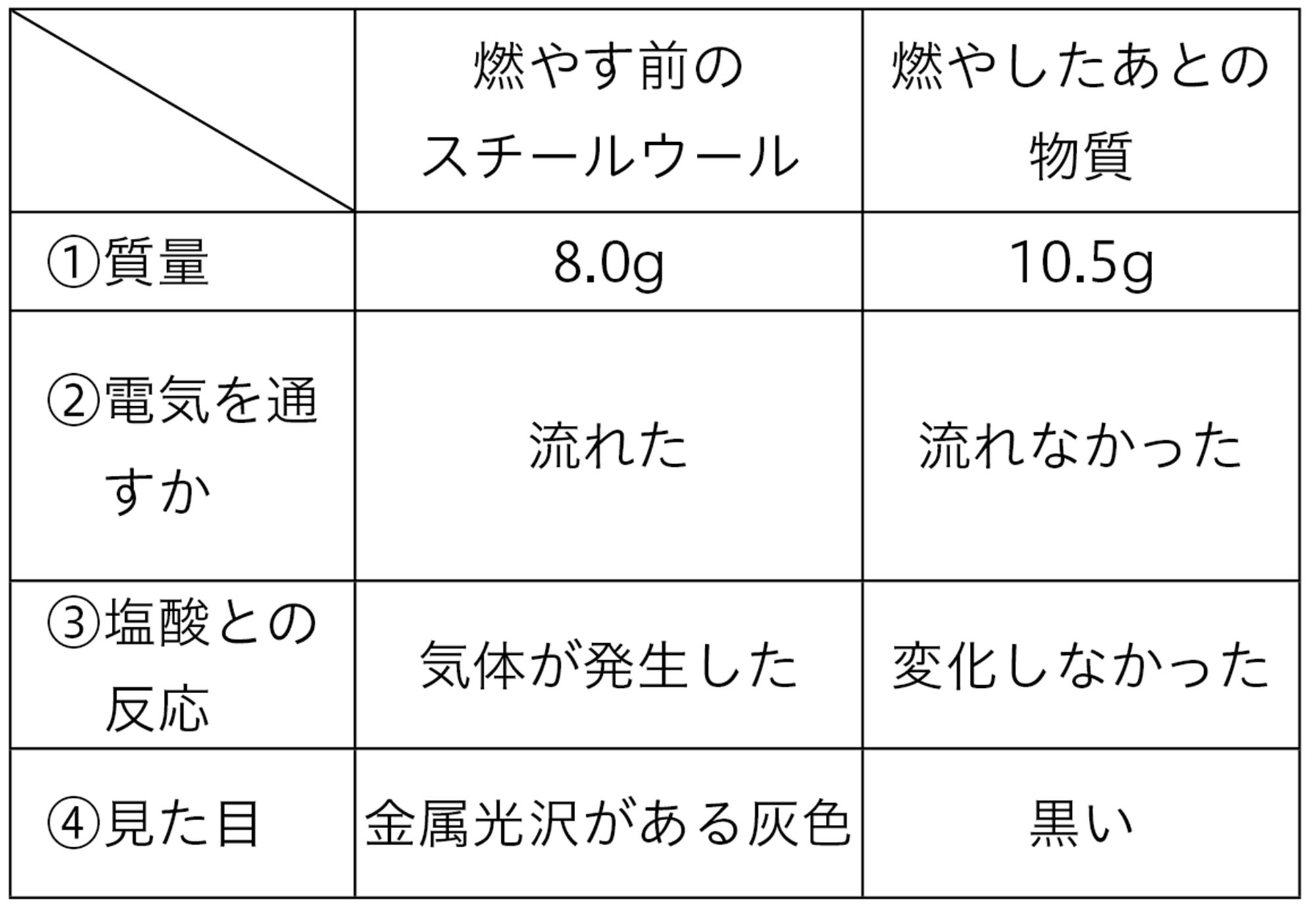
図4 探究1の結果例
- 加熱したあとの物質は,鉄とは性質が異なる。燃やすことによって,もととは異なる物質になったと考えられる。
- 鉄を加熱したあと,質量が増えていたことから,鉄に何かが結びついたと考えることができる。
※このウェブページは中学校理科2年の学習内容です。<2年p.15>
2 化学変化
探究1では,鉄を加熱すると鉄ではない物質になったことがわかる。このように,物質そのものが変化して別の種類の物質ができる変化を【化学変化】❶という。
3 酸化
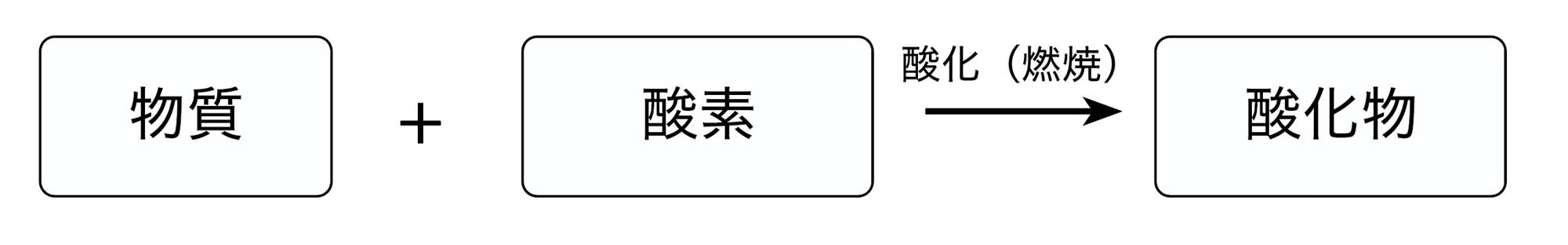
鉄を加熱してできた物質を酸化鉄といい,その質量は,もとの鉄より増えた。このとき鉄に結びついたのは,空気中の酸素である。化学変化の中でも,物質が酸素と結びつくことを酸化といい,できた物質を【酸化物】という。
また,激しく熱や光を出しながら酸化することを特に【燃焼】という。すなわち,物質が燃えるとは,物質が酸素と激しく結びつくことである。
❶ 化学反応ともいう。
※このウェブページは中学校理科2年の学習内容です。<2年p.253>
資料 食品に酸化は大敵
一般に,食品は空気中の酸素によって酸化されると,味や色が変化したり,有害な物質が生じたりするなどして質が落ちます。そのため,食品の酸化を防ぎ,長期保存するために,食品を酸素にできるだけ触れさせないくふうがされています。
たとえば,スナック菓子の袋(プラスチック製)では,袋の分子どうしの間のすき間を空気中の酸素が通りぬけないように,アルミニウムのうすい膜をはりつけている場合があります。
また,食品の袋の中に,酸素を取り除く脱酸素剤を入れてある場合もあります。一般的な脱酸素剤には,食品よりも酸化されやすい鉄粉が入っています。
食品添加物として「酸化防止剤」が食品や飲料水に入れられることもあります。酸化防止剤は,酸化されやすい物質からできており,食品の代わりとなって酸化されることにより,食品そのものの酸化を防止します。
※このウェブページは中学校理科2年の学習内容です。<2年p.16>
4 原子
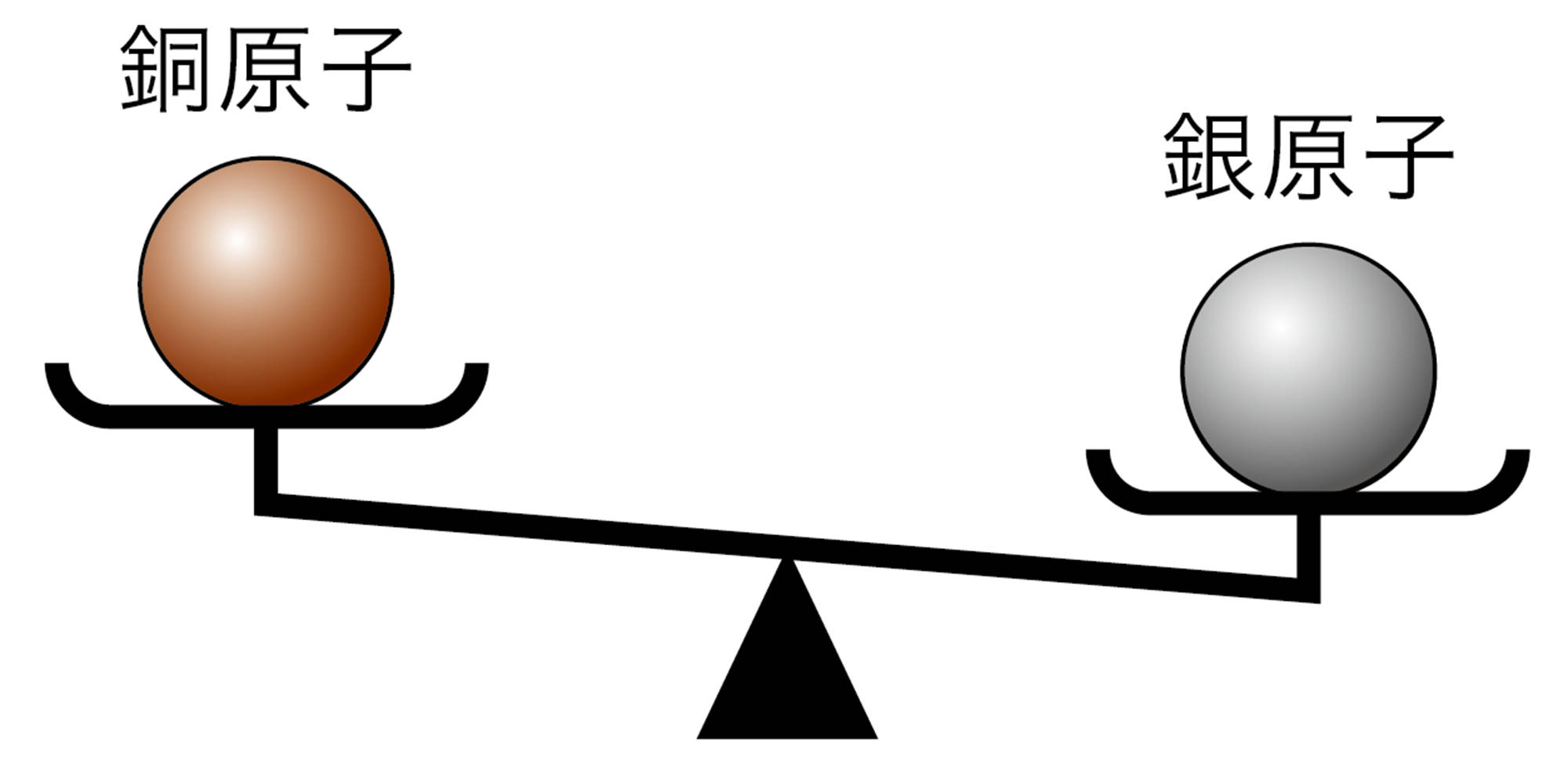
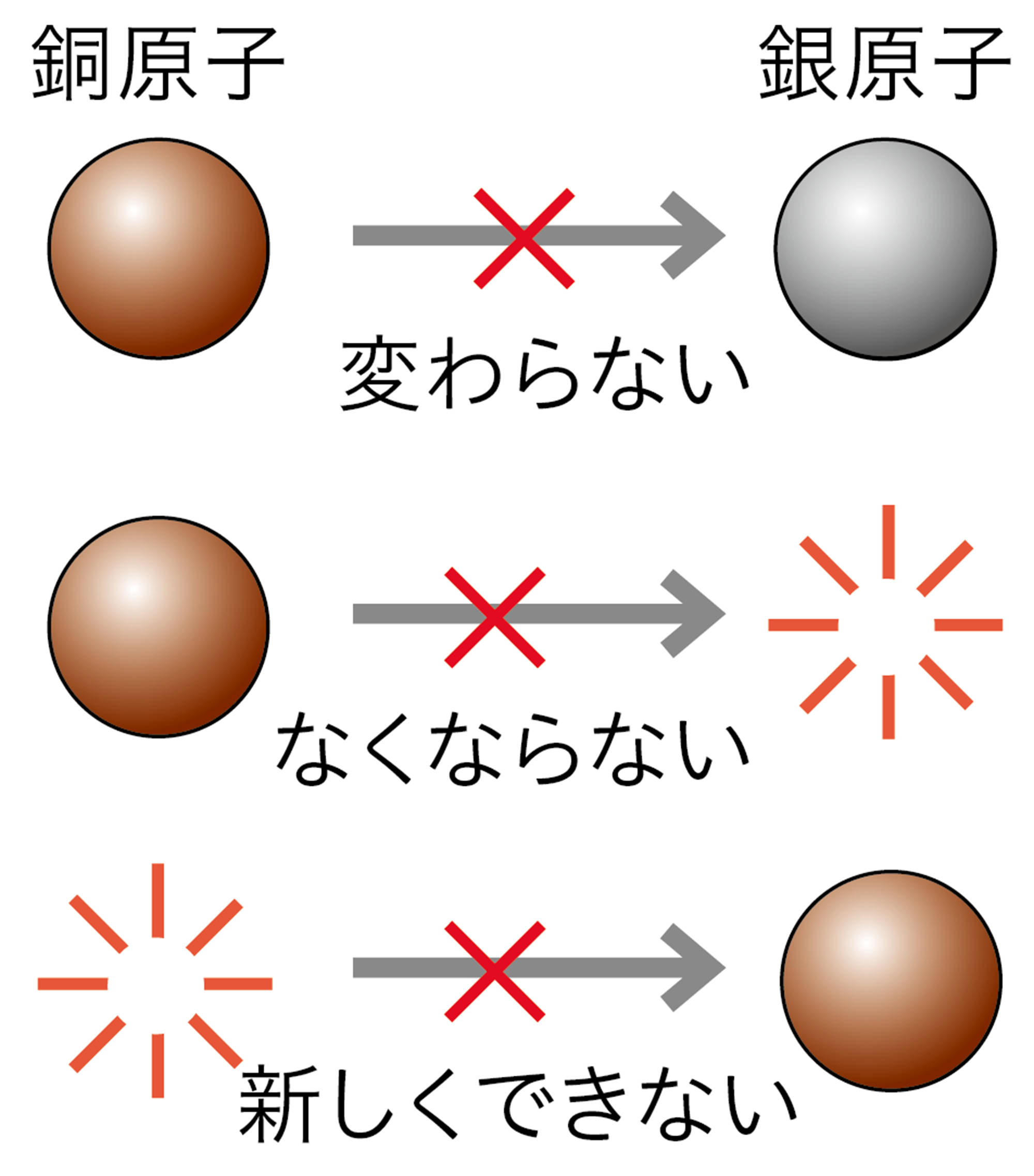
化学変化のときの質量の変化などを手がかりに,物質のなりたちにせまった一人が,イギリスの科学者ドルトンである。ドルトンは,すべての物質はそれ以上分割することのできない小さな粒子からできていると考え,その粒子を【原子】とよんだ。原子には図6 のような性質があることがわかっている。
図6 原子の性質
5 元素
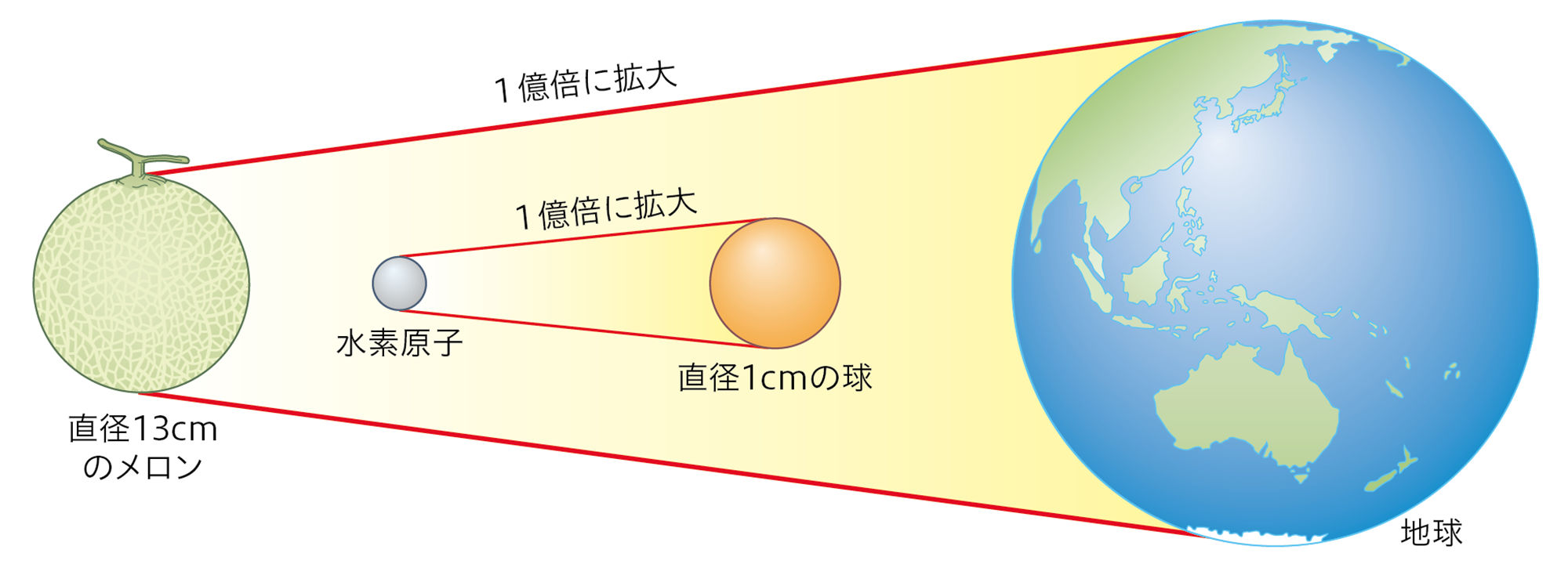
現在,すべての物質は原子からできていることが確かめられている。原子は100種類以上あり,原子の大きさや質量は原子の種類によってちがう。原子は,その構造をもとに原子番号がつけられていて,おおよそ原子番号の順に原子1個の質量は大きくなっていく。また,物質を構成する原子の種類のことを元素という。
※このウェブページは中学校理科2年の学習内容です。<2年p.252>
発展 原子の内部(中学3学年で学習)
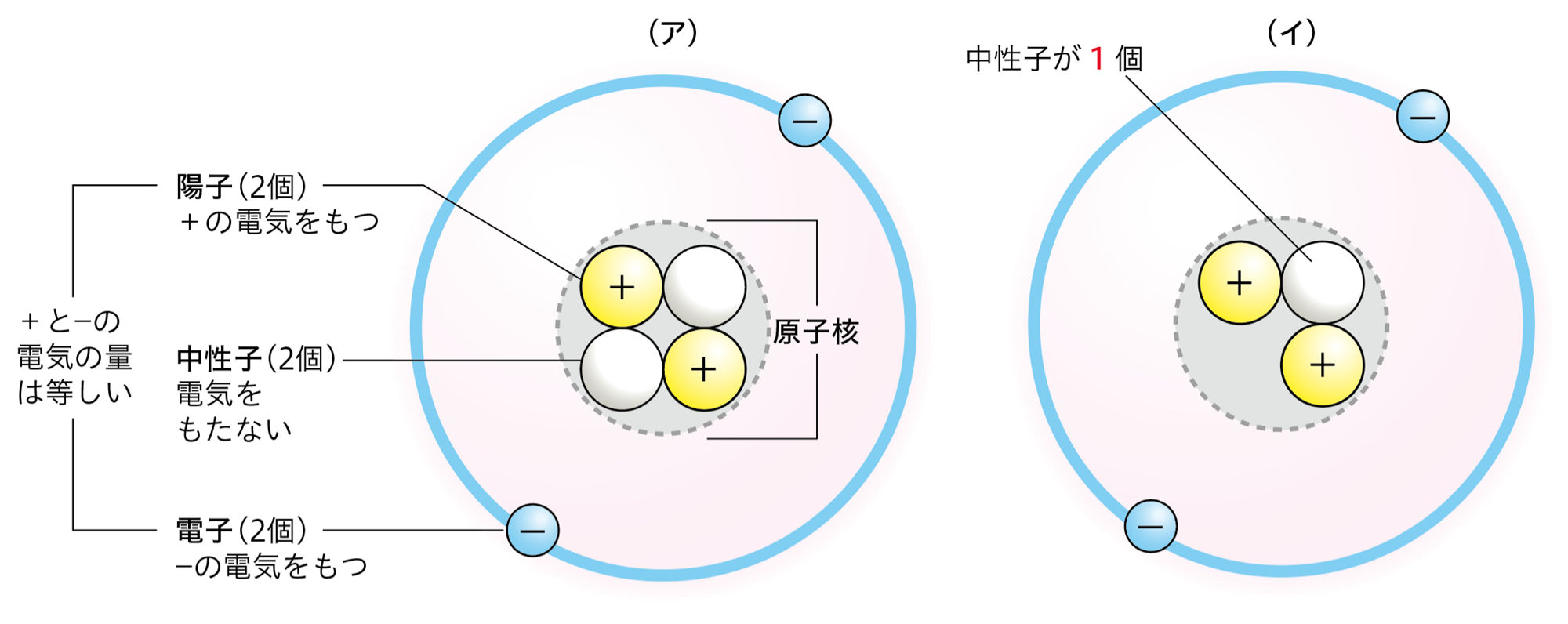
原子は,さらに小さい粒子(図(ア)のような,+の電気をもつ原子核と,− の電気をもつ電子)をもっていることがわかっている。原子核は原子の中心にあり,そのまわりに電子が存在する。また,原子核は,+の電気をもつ陽子と,電気をもたない中性子が集まってできている。
周期表で表されている原子番号は,その原子がもつ陽子の数である。ヘリウムの原子番号は2であり,これは2つの陽子をもつことを表している。また,自然界にあるヘリウム原子のほとんどは,(ア)のように中性子を2つもっているが,ごくわずかに(イ)のように中性子を1つもっているものもある。(ア)と(イ)をまとめて「ヘリウムの元素」という。
※このウェブページは中学校理科2年の学習内容です。<2年p.17>
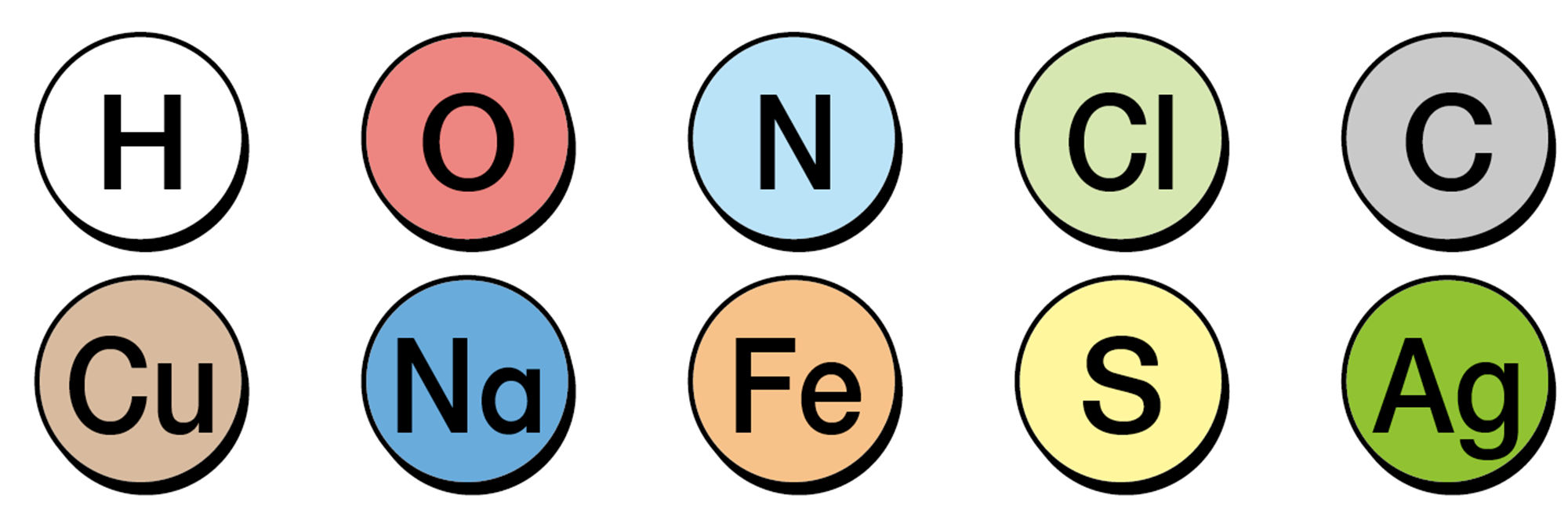
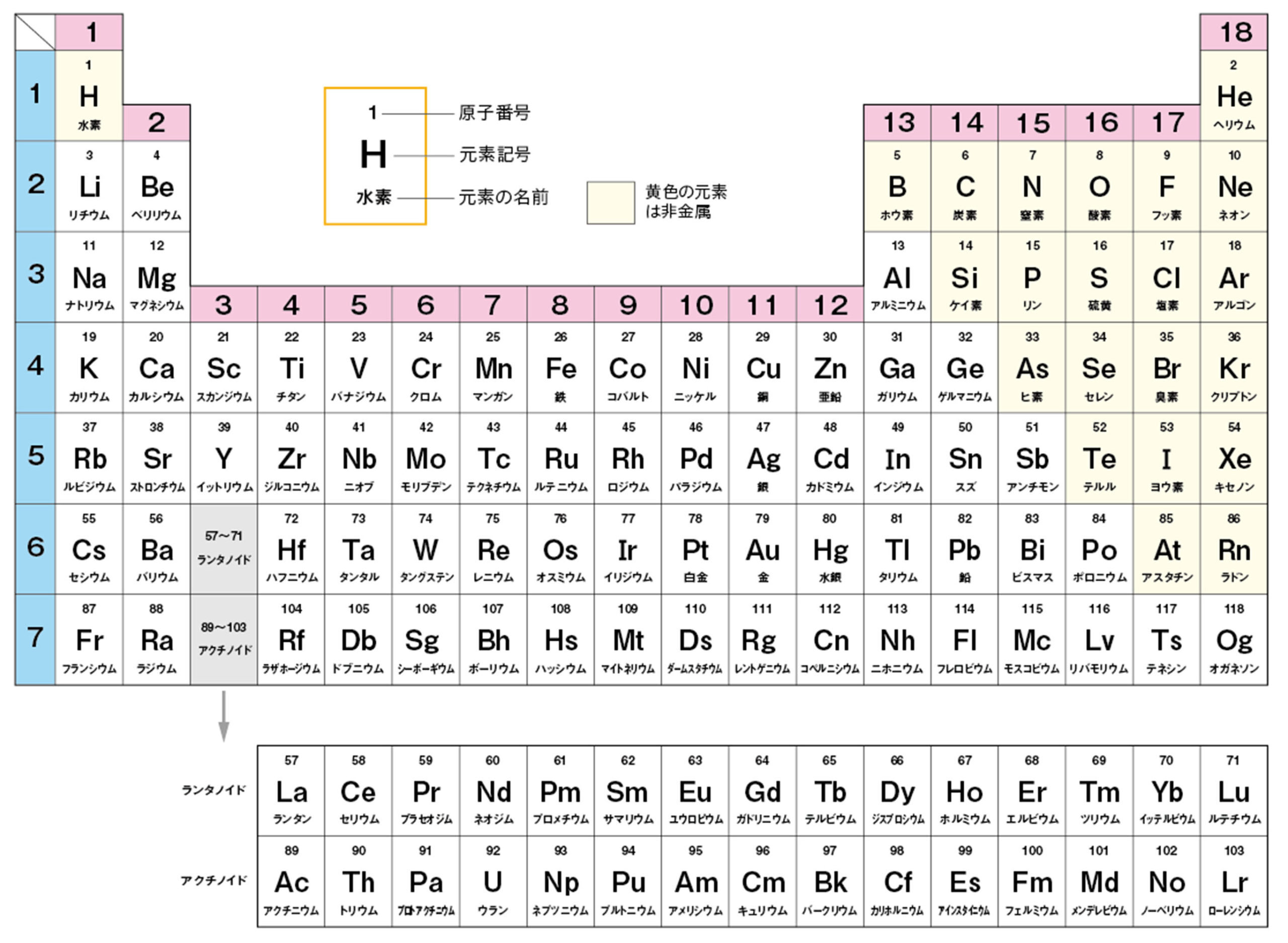
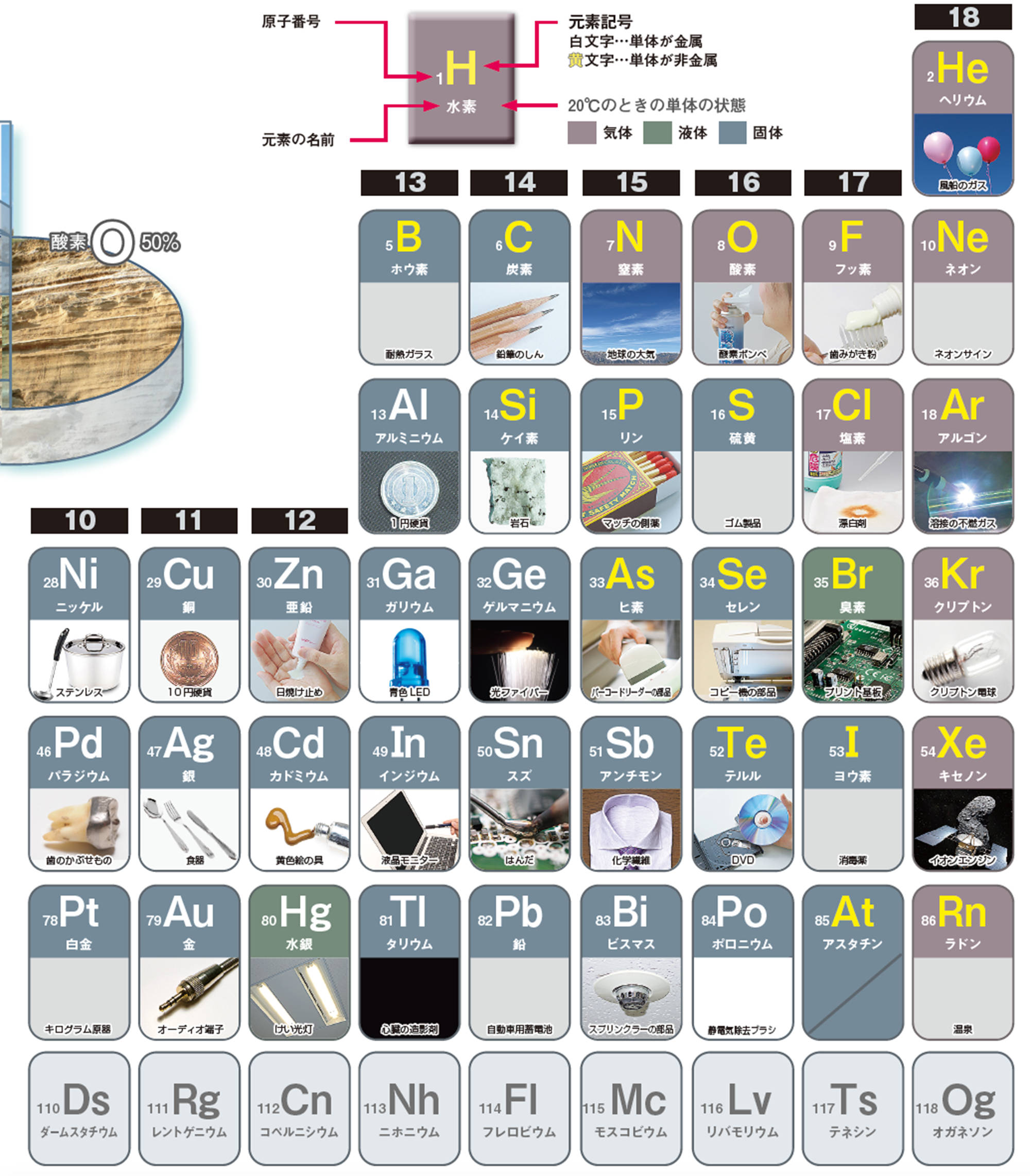
6 元素記号と周期表
元素にはそれぞれ記号が決められていて,アルファベット1文字または2文字で表される(図9)。この記号を【元素記号】とよび,世界で共通に使われている。元素を原子番号などにもとづいて整理した表を【周期表】という(図11)。周期表では,性質の似た元素が縦にならぶ。
次の物質は中学校でよく出てきます。 周期表で元素記号を覚えておきましょう。
金属 ナトリウム,マグネシウム,アルミニウム,カリウム,カルシウム,鉄,銅,亜鉛,銀,バリウム,金
非金属 水素,ヘリウム,炭素,窒素,酸素,塩素,ケイ素,硫黄


原子の考えは古代からありました。しかしそれが科学的になったのは19世紀です。18世紀後半に精密な上皿てんびんを使って,質量を正確に調べる実験が行われるようになり,19世紀の初頭にドルトンが唱えた原子説は,化学変化における質量の変化などが根拠にされました。

ドルトン(イギリス,1766〜1844年)
ただし,原子を観察できるわけではなかったので,原子説は,長い間仮説として考えられていました。その後,原子があるとしか考えられない現象が集まってきて,原子説は受け入れられていきます。今では,特殊な顕微鏡(→p.8)によって,原子1粒を撮影することができます。

原子カードに磁石を貼っておくと,黒板などにつけられるから,みんなで話し合うときに便利だね。


さっそく,次の探究2から使ってみましょう。下のウィンドウから原子カードアプリも利用できます。
※このウェブページは中学校理科2年の学習内容です。<2年p.252>
資料 周期表は計画通り
19世紀にイギリスのドルトンにより原子説が提唱されたあと,いろいろな元素が明らかになり,それぞれの元素の原子の質量が実験の積み重ねにより知られるようになってきました。
19世紀になると,ロシアの科学者メンデレーエフは,元素を原子の質量の小さい方から順にならべたとき,似た性質をもつ異なる元素が,周期的にくり返し現れることに気がつきました。
メンデレーエフは,表の縦の列に似た性質の元素がならぶように工夫した元素周期表を考案しました。彼が考案した周期表には,空欄がいくつも生じましたが,あえて空欄としました。空欄にぴったり当てはまる質量や性質をもった未発見の元素があるはずだと考えたのです。
その後,多くの元素が発見されて表の空欄がうまっていきました。それらの元素は,彼の予想通りの原子の質量や性質だったので,人々を驚かせました。
メンデレーエフの周期表がもとになり,修正が加えられていくことにより,現在の周期表ができていきました。高校以降でくわしくあつかいますが,周期表には,元素の性質を整理してとらえることができる,さまざまなヒントが隠されています。
発展
周期表をもとにして元素の性質を整理してとらえることのできる例を2つあげる。
- アルカリ金属 周期表の左端の列にならぶ,リチウム,ナトリウム,カリウム…は,非常に化学反応を起こしやすい金属で,水に触れただけで激しく反応してアルカリ性の水溶液になる性質が共通しており,「アルカリ金属」とよばれる。
- 貴ガス(希ガス) 周期表の右端の列にならぶ,ヘリウム,ネオン,アルゴンといった元素は,他の原子と結びつきにくく原子1個ずつばらばらの状態で気体を構成する性質が共通し,「貴ガス」とよばれる。
※このウェブページは中学校理科2年の学習内容です。<2年p.253>
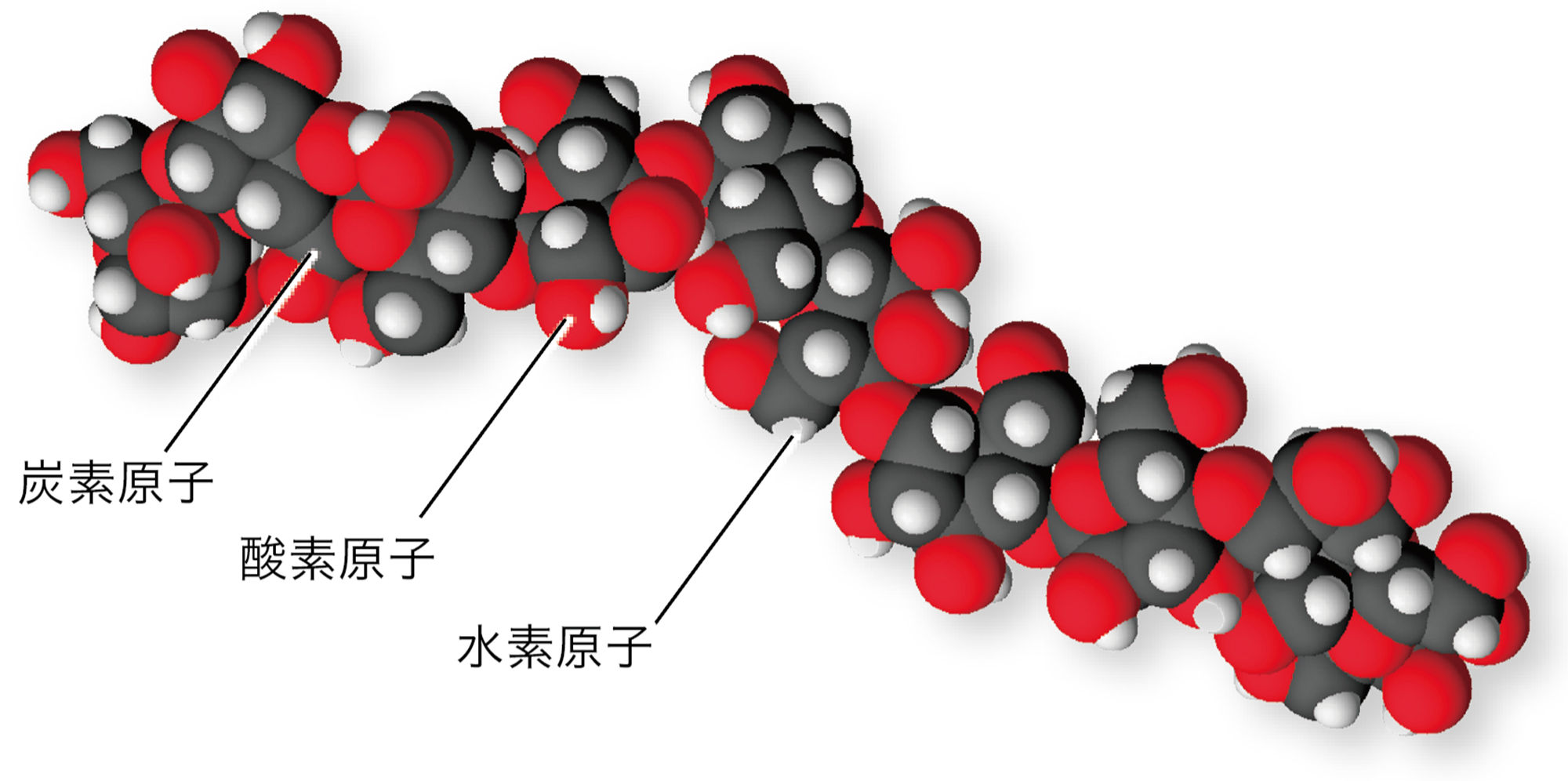
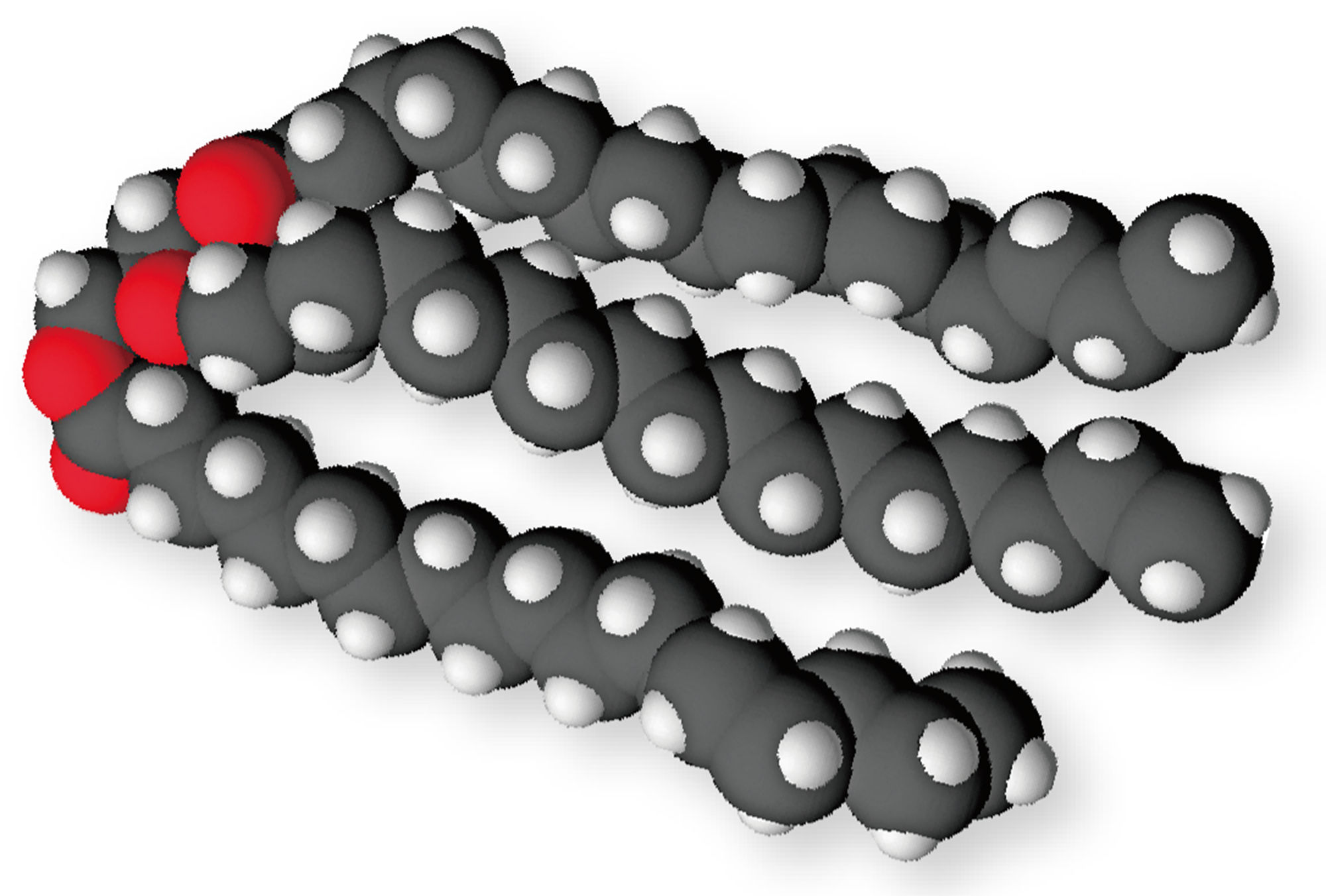
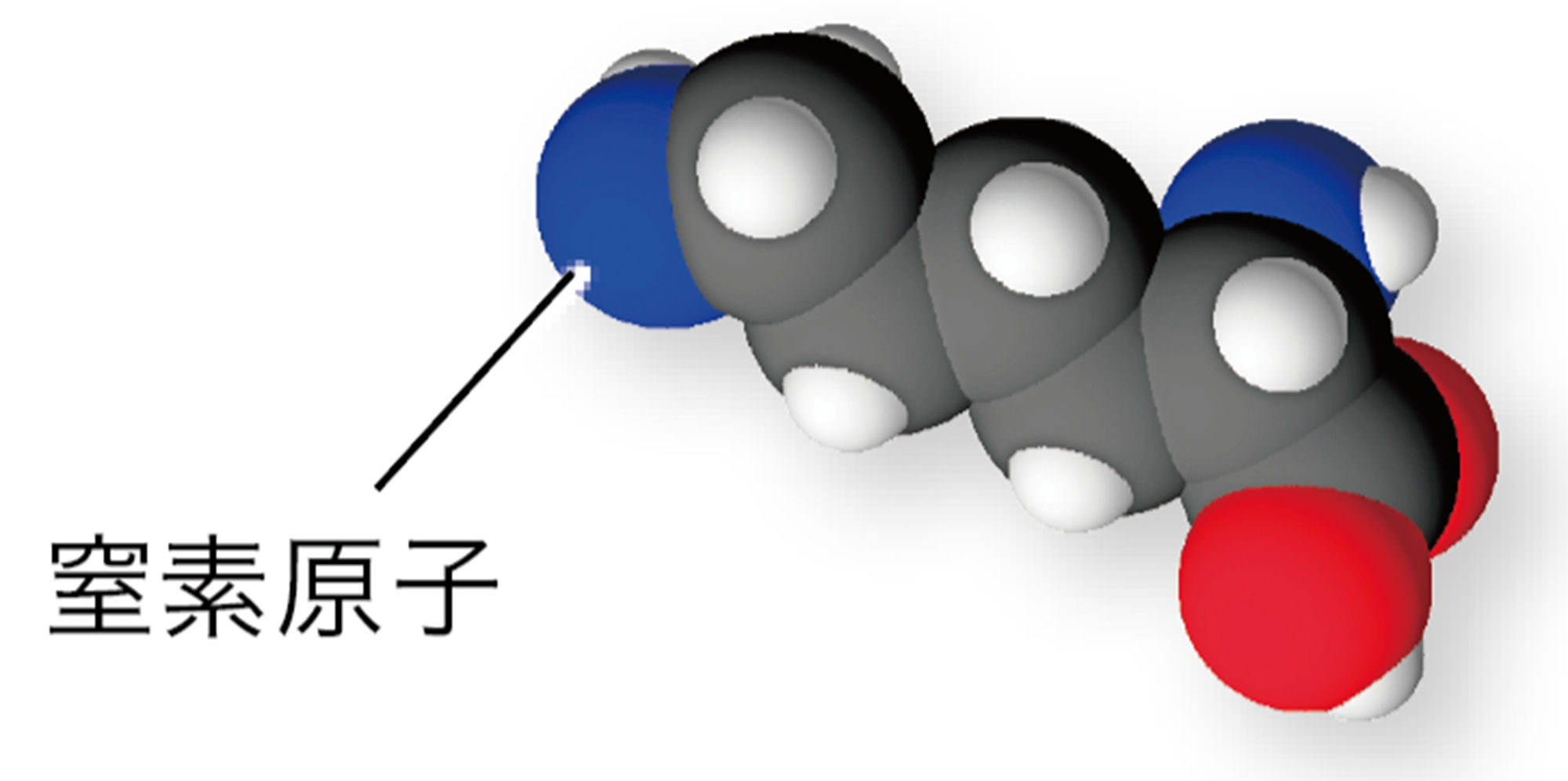
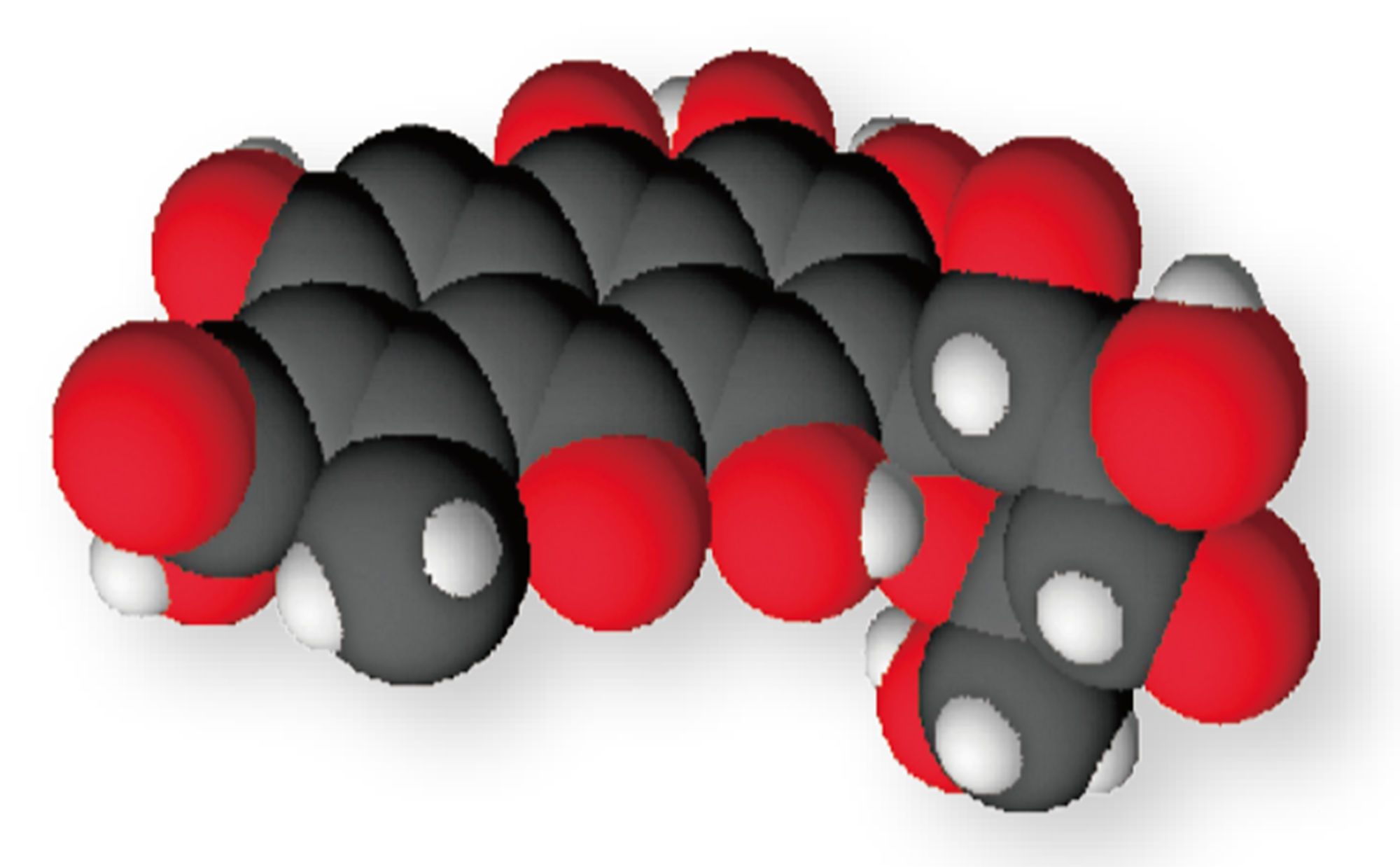
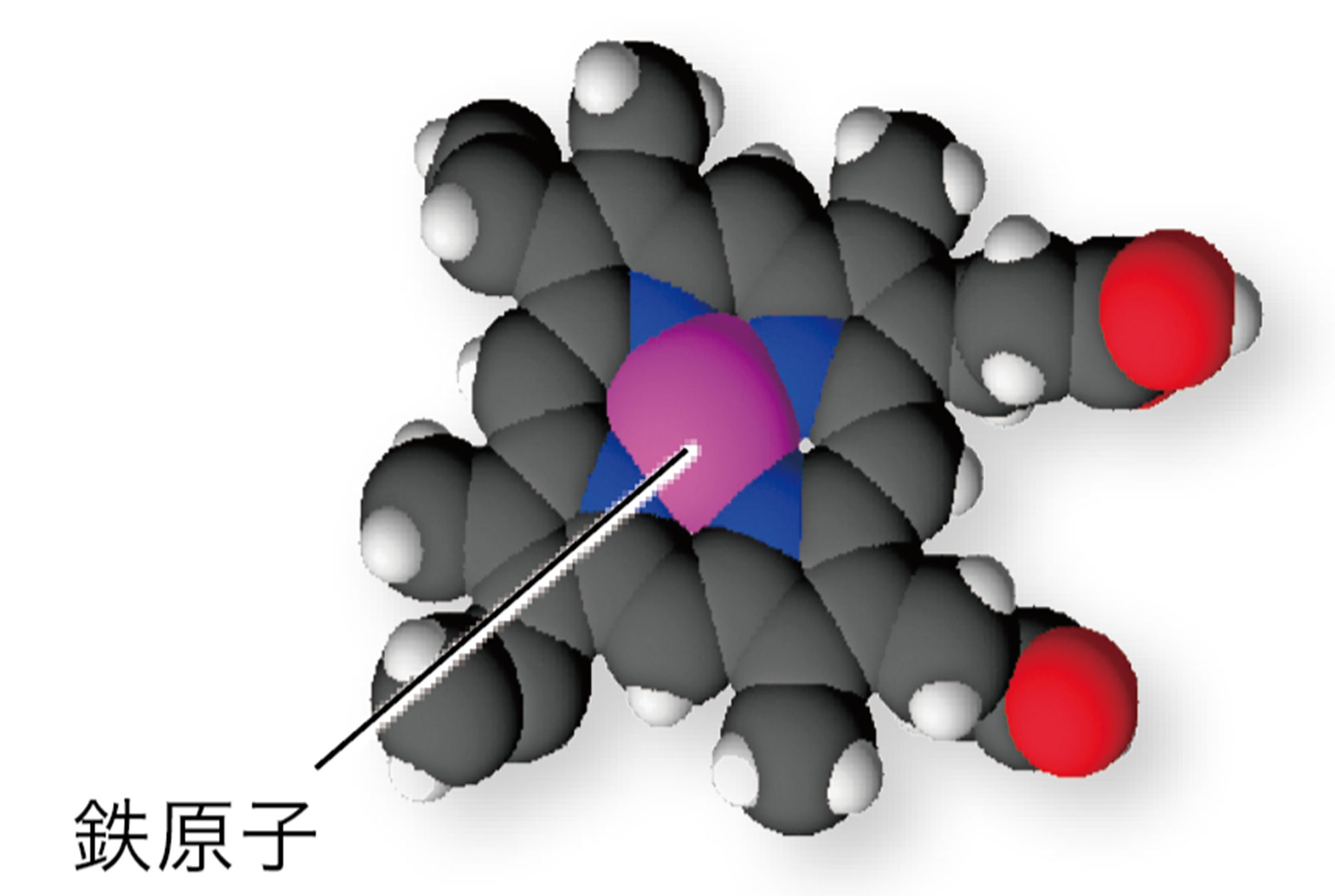
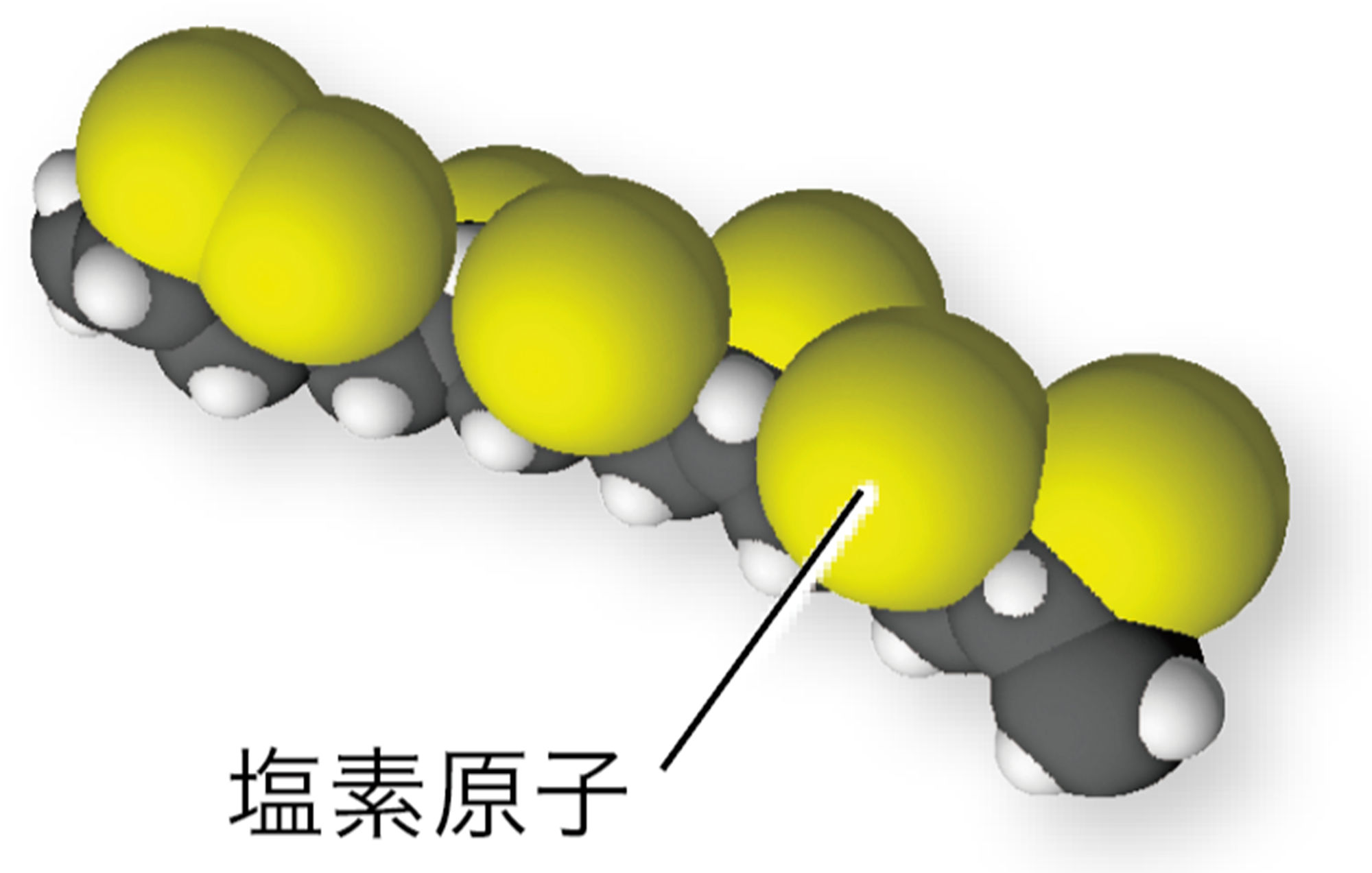
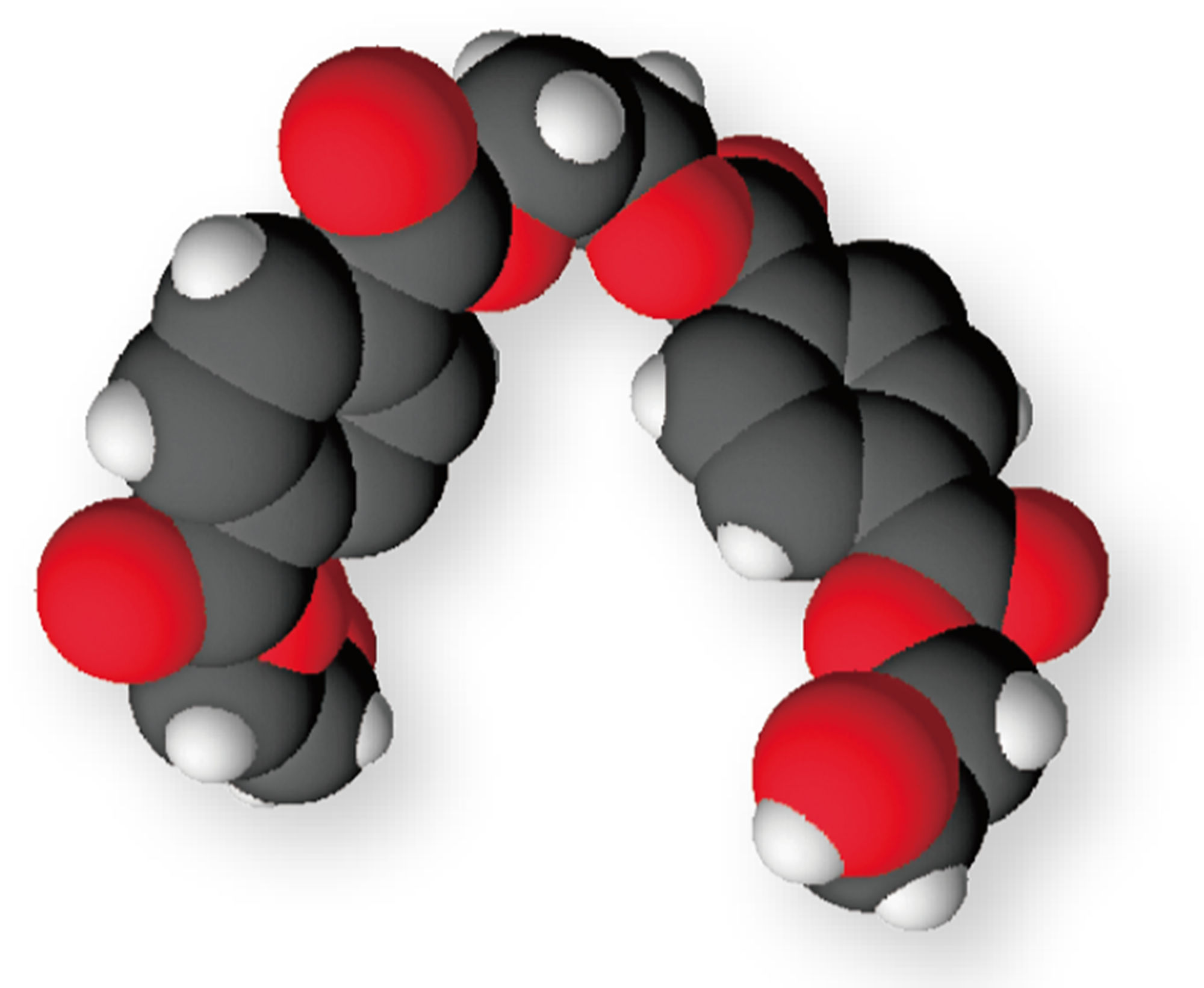
発展 大きな分子
化合物の種類が非常に多いのは,非常に多くの原子が組み合わさってできた分子の存在が理由のひとつである。たとえば下図のような分子があり,これらがたくさんつながった状態を「高分子(高分子化合物)」とよぶ。特に炭素原子は他の原子との結びつきの数(→p.24)が4つと多く,炭素原子どうし,あるいはほかの原子といろいろな組み合わせで結合することができる。高分子化合物のなかでも,炭素原子が多数連なったつくりをもつ分子を「有機高分子化合物」という。
※このウェブページは中学校理科2年の学習内容です。<2年p.19>
7 物質の結びつきと原子
物質の性質や変化を原子のモデルで考えたとき,鉄が燃えることは,鉄と酸素の原子が結びつくと表現することができる。では,その他の2種類の物質による化学変化について,どのように科学的に探究できるだろうか。
探究2 物質を加熱して分類する

温泉にこのような貼り紙がありました。これを化学変化という見方で考えていきましょう。
「黒ずんでしまう」ということは,鉄の酸化みたいに「さび」ができるんでしょうか?

図12 硫黄をふくむ温泉の貼り紙
鉄と硫黄が結びつく化学変化は,原子のモデルでどのように説明できるか。

今度は原子のモデルで説明できるよ。鉄はFe,硫黄はSだね。
物質が結びつくようすを原子カードで表してみよう。


硫黄と鉄が結びついて,ちがう性質の物質になるのかな?

最初にあった金属が,化学変化で異なる物質になったことを確かめるには,どうすればよいだろう。
探究1が参考になるね。金属の性質を確認しよう。


この実験では,気体や水は出ないのかな?確かめる方法も取り入れた方がいいんじゃないかな。
※このウェブページは中学校理科2年の学習内容です。<2年p.20>
準備
スチールウール(鉄),硫黄の粉末,塩酸(5%),試験管(4),試験管ばさみ,薬さじ,試験管立て,磁石,ガラス棒,加熱器具,スポイト,脱脂綿,薬包紙,保護めがね
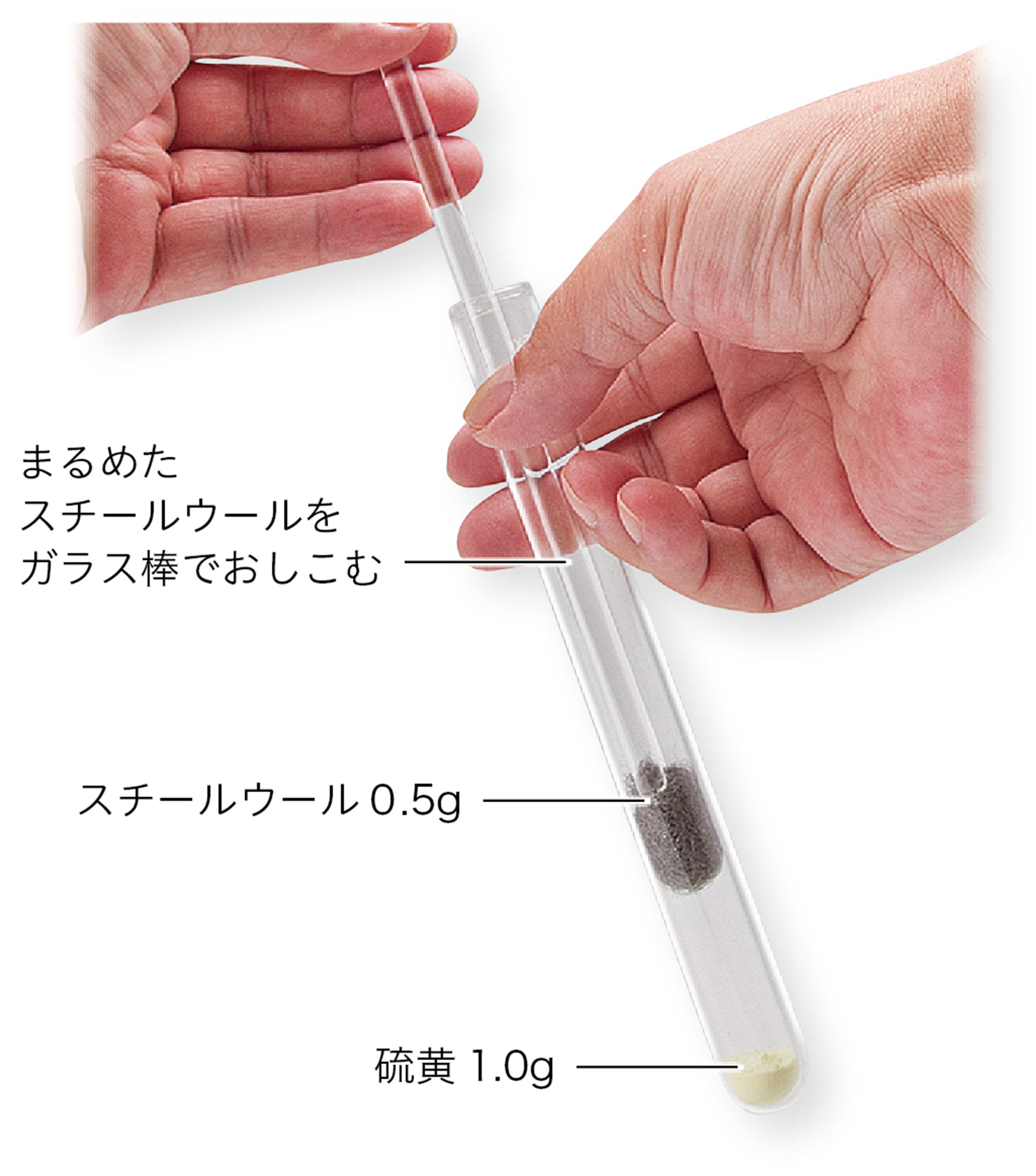
1.硫黄と鉄を試験管に入れる
試験管に硫黄の粉末を1.0g入れ,その上にスチールウール0.5gを入れる。硫黄の蒸気(気体)が出るのを防ぐため,試験管の口を脱脂綿で軽くふさぐ。
注意!! 実験は換気をよくして行う。発生する気体を吸いこまない。
2.加熱する
試験管を加熱し,赤くなったら加熱をやめ,変化のようすを観察する。
注意!! 加熱するときは,試験管ばさみを使う。試験管が熱くなるので,やけどしないように気をつける。
3.加熱する前後の物質を調べる①
加熱後の物質を,薬さじなどで試験管から取り出す。
反応前のスチールウールと,加熱後に取り出した物質について,色や手ざわり,磁石へのつき方を比べる。
ポイント
弱い磁石を使うと,ちがいがわかりやすい。
※このウェブページは中学校理科2年の学習内容です。<2年p.242>
基本操作 ガスバーナーの使い方
注意!! 火を消した直後は,ガスバーナーの口の付近は熱くなっているので,さわらないよう注意する。
※このウェブページは中学校理科2年の学習内容です。<2年p.21>
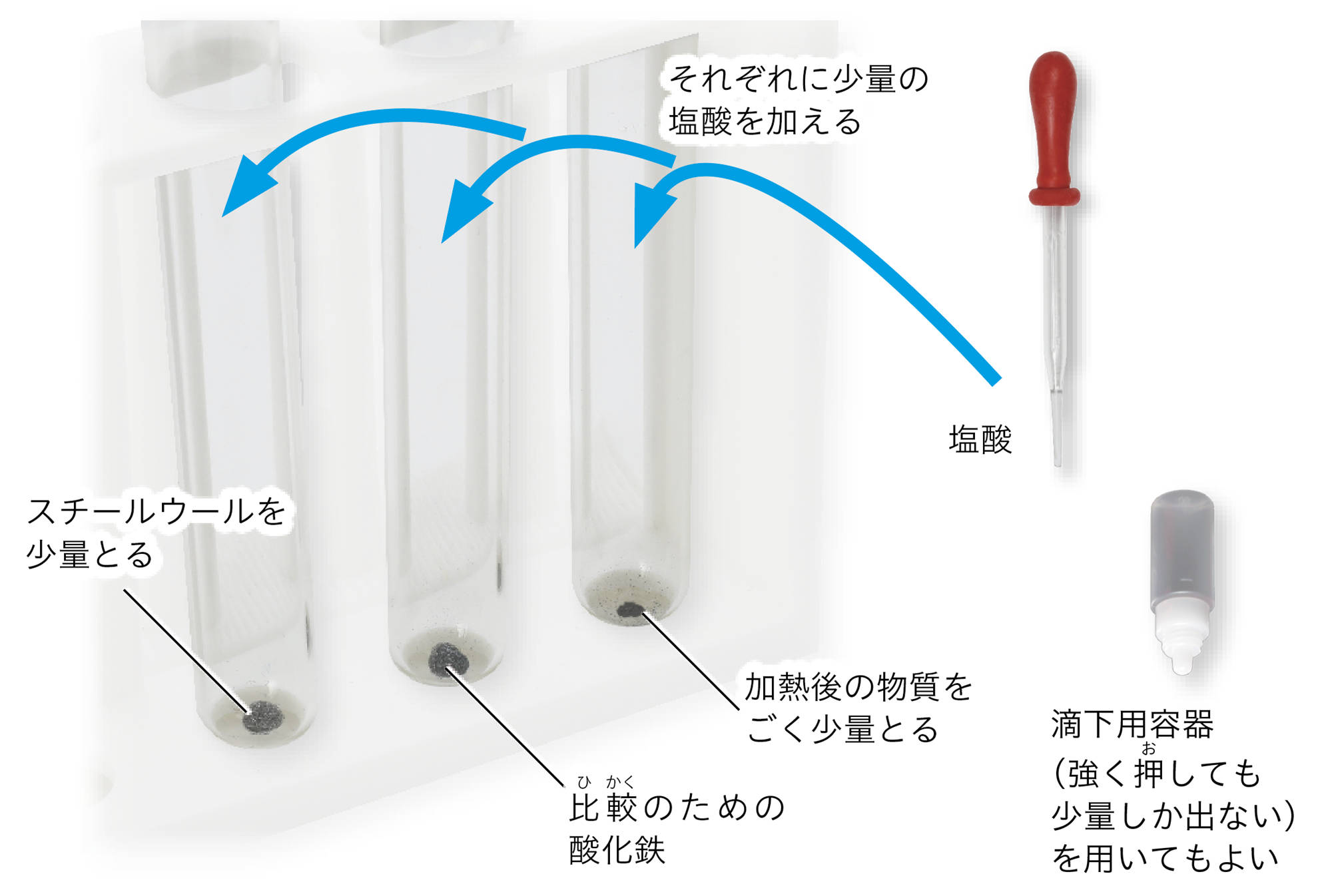
4.加熱する前後の物質を調べる②
加熱前と後の物質を試験管に少量とり,うすい塩酸を数滴(先生が決めた量)加え,発生する気体のにおいを比べる。
ポイント
- 加熱の前後で,物質の色,磁石へのつき方はどのようにちがったか。
- 加熱の前後で,物質に塩酸を加えたときの気体の発生のしかたやにおいはどのようにちがったか。
ポイント
- 加熱によってスチールウールは別の物質に変わったといえるか。その理由は何か。
- この実験の化学変化をFe,Sの原子カードを使って表す。
※このウェブページは中学校理科2年の学習内容です。<2年p.22>
探究2 結果から考察する
「卵のくさったようなにおい」とは,硫黄温泉の近くでただようにおいです。

硫黄と反応した鉄は,もとの鉄とは性質が異なっていた。原子のモデルを用いると,次のように考えられる。
鉄原子を●,硫黄原子を○とすると,
探究2の化学変化は
●+◯→●◯
と表せる(ただ● ◯ではなく,●と◯が結びついている)。
❶ 結果をわかりやすくするために,塩酸の量を増やして撮影している。実際は塩酸を多く加えない。
※このウェブページは中学校理科2年の学習内容です。<2年p.23>
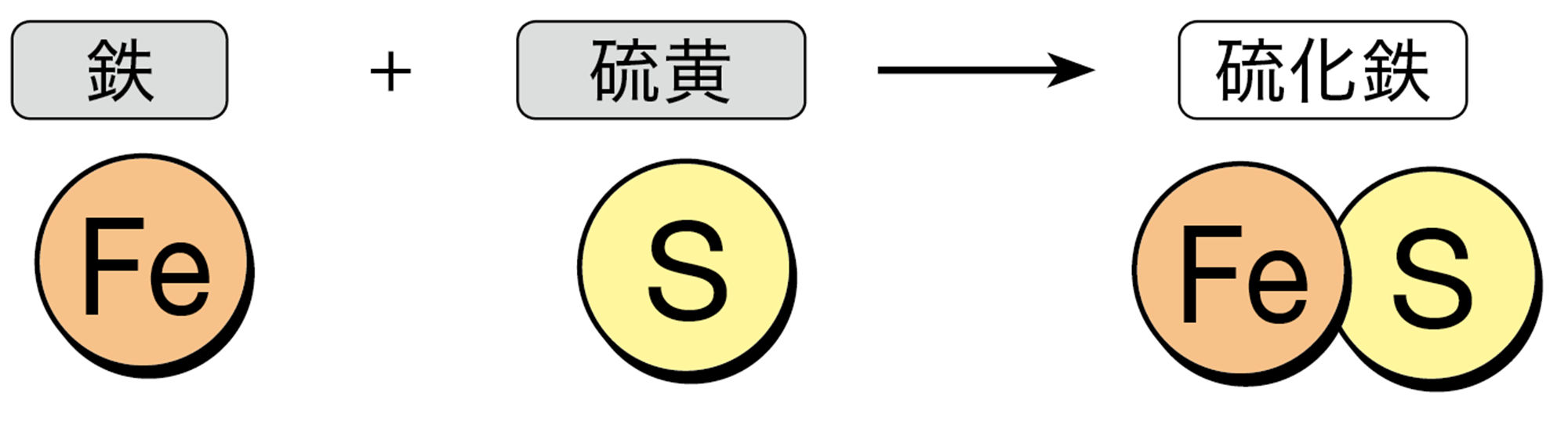
鉄と硫黄をいっしょに加熱すると,光と熱を出す激しい反応が起こる。この反応によって生じた物質は,探究2の結果から,もとのスチールウール(鉄)とは異なる物質であることがわかる❶。
この化学変化では,鉄Feと硫黄Sが結びついて,硫化鉄FeSという物質ができる❷。
❶ 硫黄は,磁石につかず,塩酸を加えても変化しない。このことから,探究2の加熱後の物質は,硫黄とも異なる物質であることがわかる。
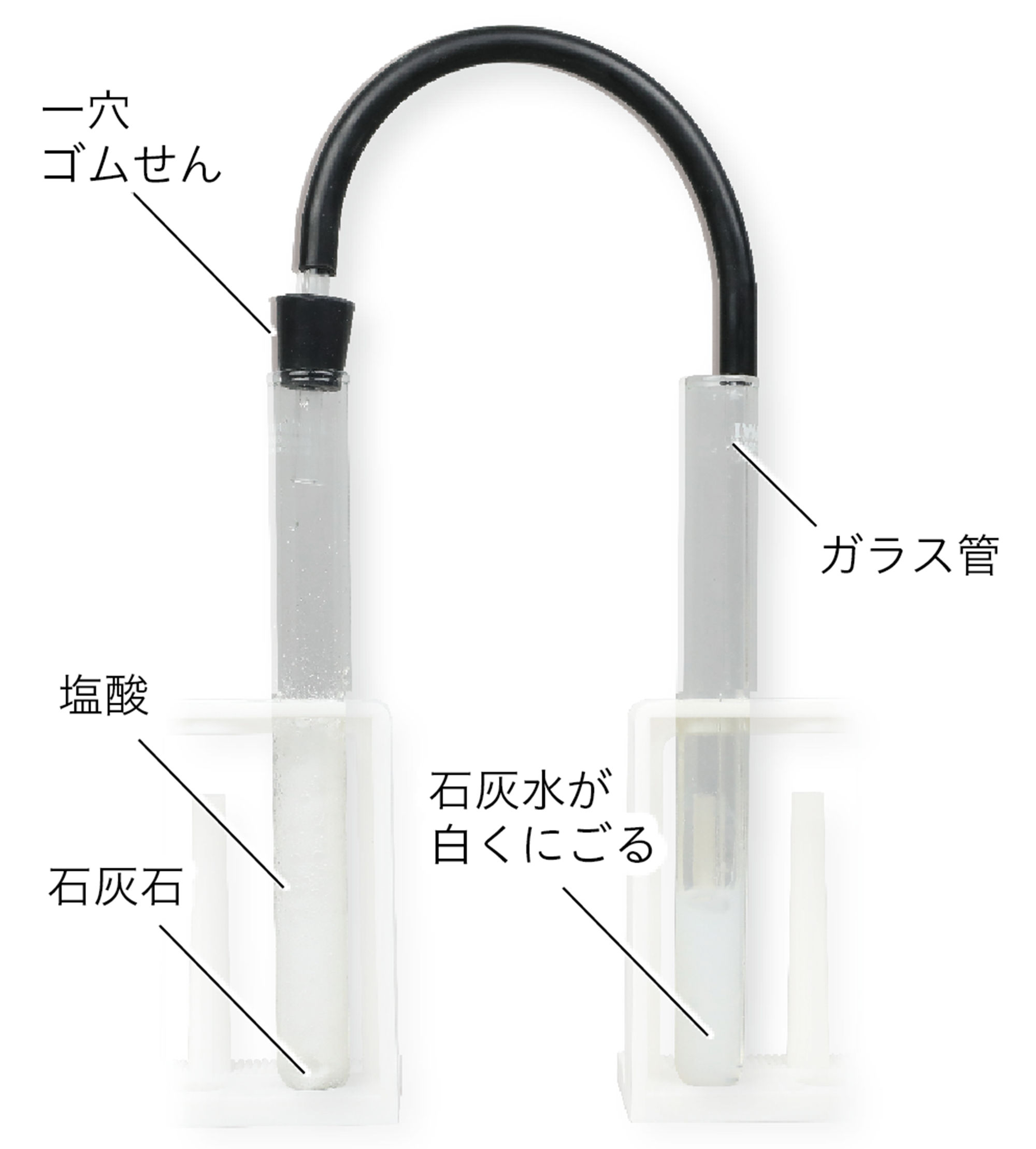
❷ 硫化鉄に塩酸を加えると,硫化鉄FeSのSと,塩酸HClのHが結びついて,硫化水素ができる。![]()
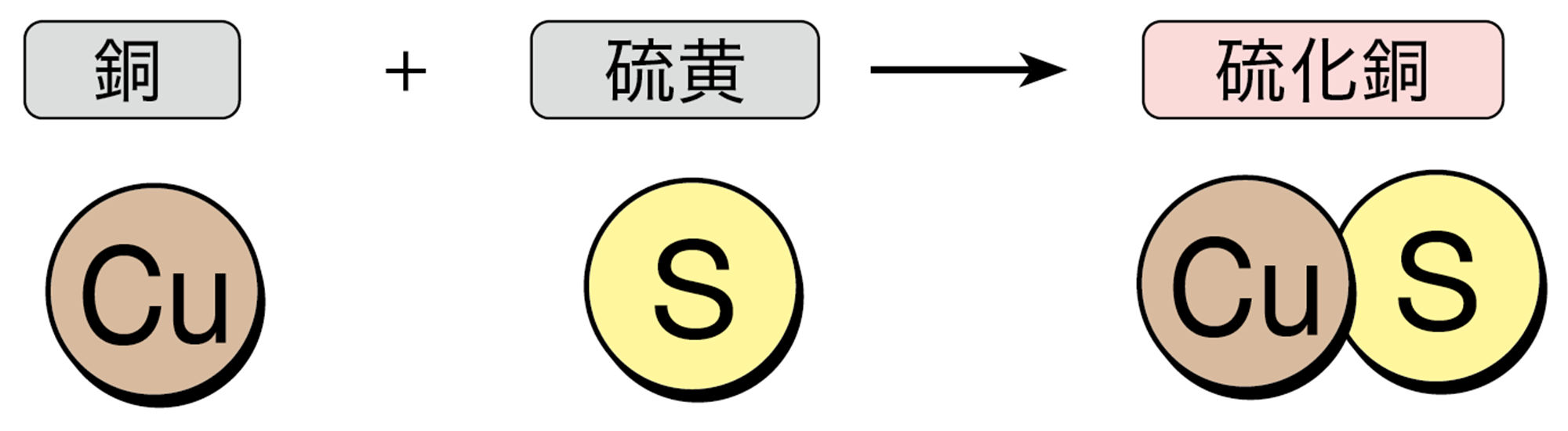
銅と硫黄をいっしょに加熱すると,銅と硫黄が結びついて硫化銅CuSができます。

8 単体と化合物
FeやCuのように1種類の原子からできている物質を単体という。酸化鉄や硫化鉄などのように,2種類またはそれ以上の種類の原子が結びついてできている物質を化合物という❸。
主な原子は100種類程度であるが,これまでに発見された物質は,原子の種類よりはるかに多い2 億 6000 万種類以上もある。これは原子がさまざまな組み合わせで結びつき,化合物をつくるからである。
❸ 鉄に酸素や硫黄が結びつくように,2つ以上の物質が結びつく化学変化を「化合」とよぶこともある。
図14 特殊な顕微鏡で撮影した単体・化合物
※このウェブページは中学校理科2年の学習内容です。<2年p.24>
9 分子
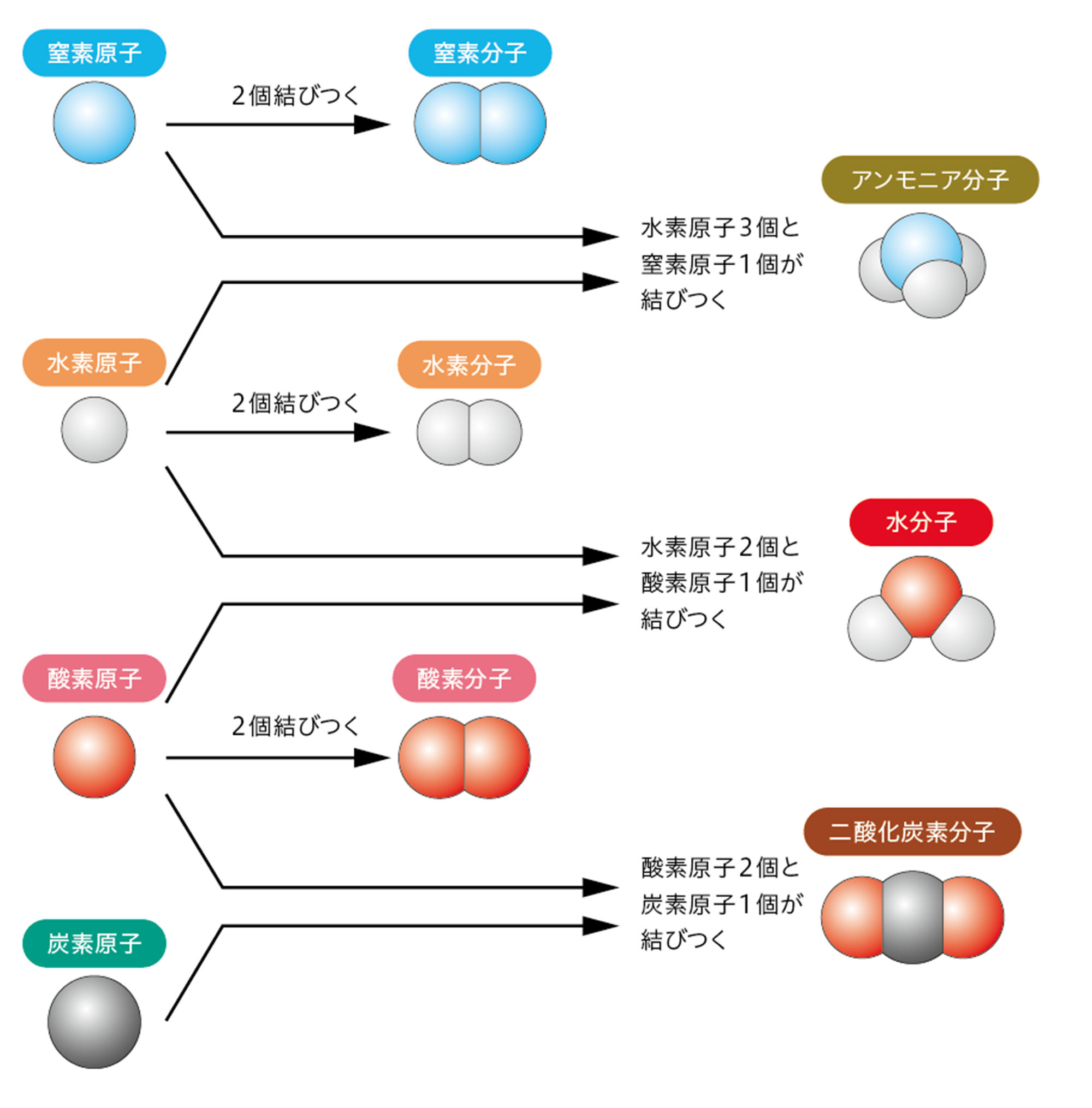
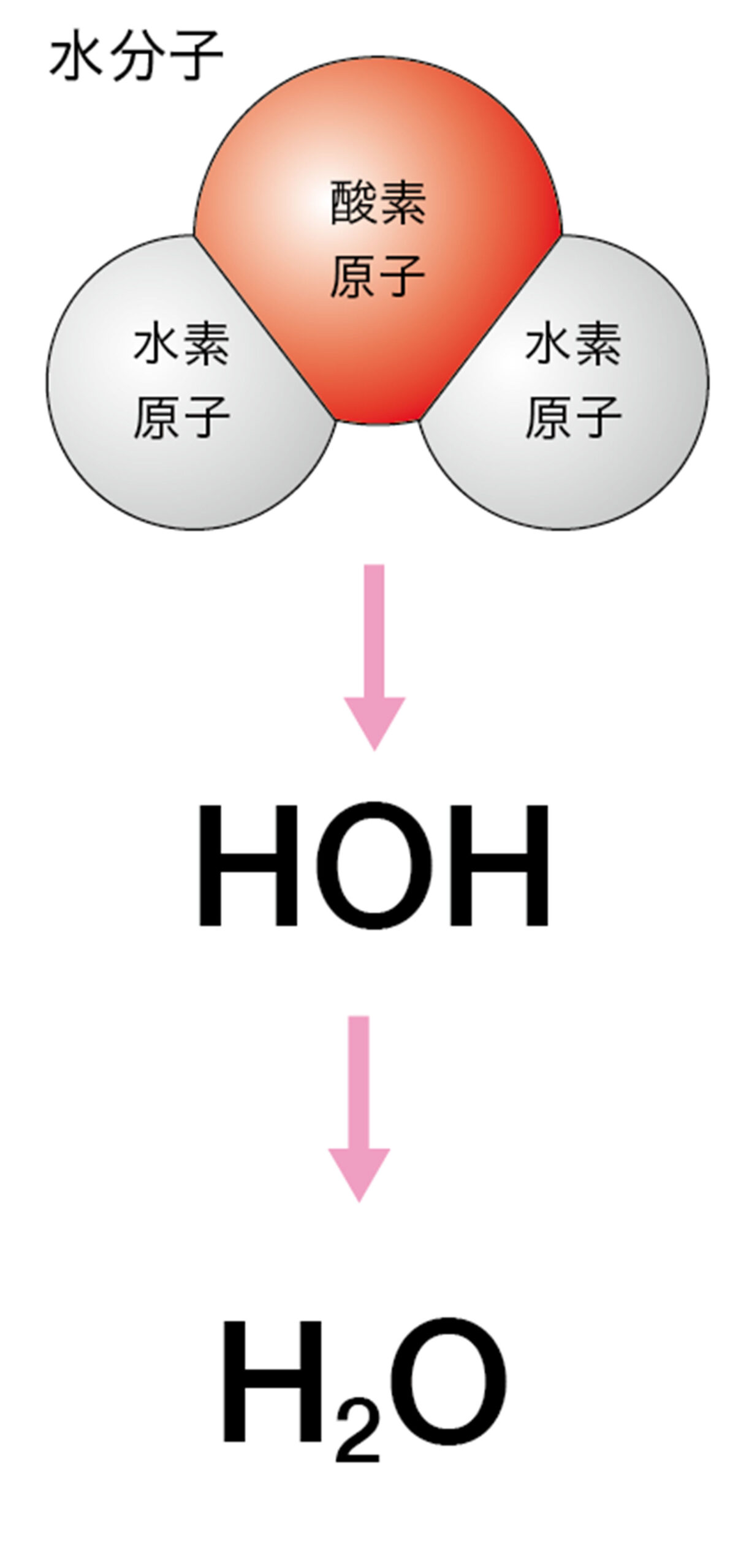
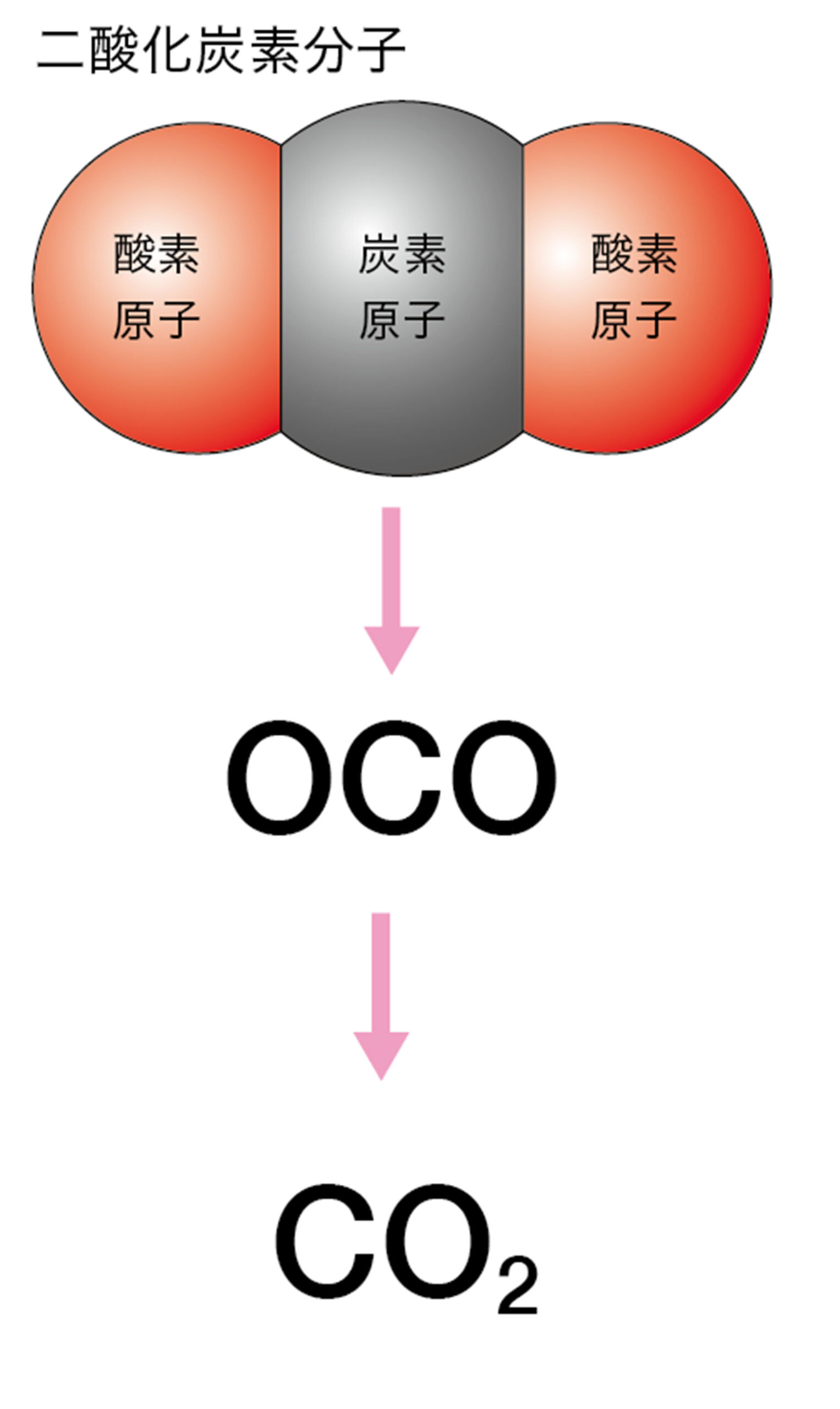
酸素や水素などの気体では,原子が単独に存在するのではなく,いくつかの原子が結びついた粒子が1つの単位になっている。この粒子を【分子】❶とよぶ(図15)。
水素分子や酸素分子などのように,1種類の原子からできている物質は「分子をつくる単体」です。水分子やアンモニア分子などのように,2種類またはそれ以上の種類の原子が結びついてできている物質は「分子をつくる化合物」です。

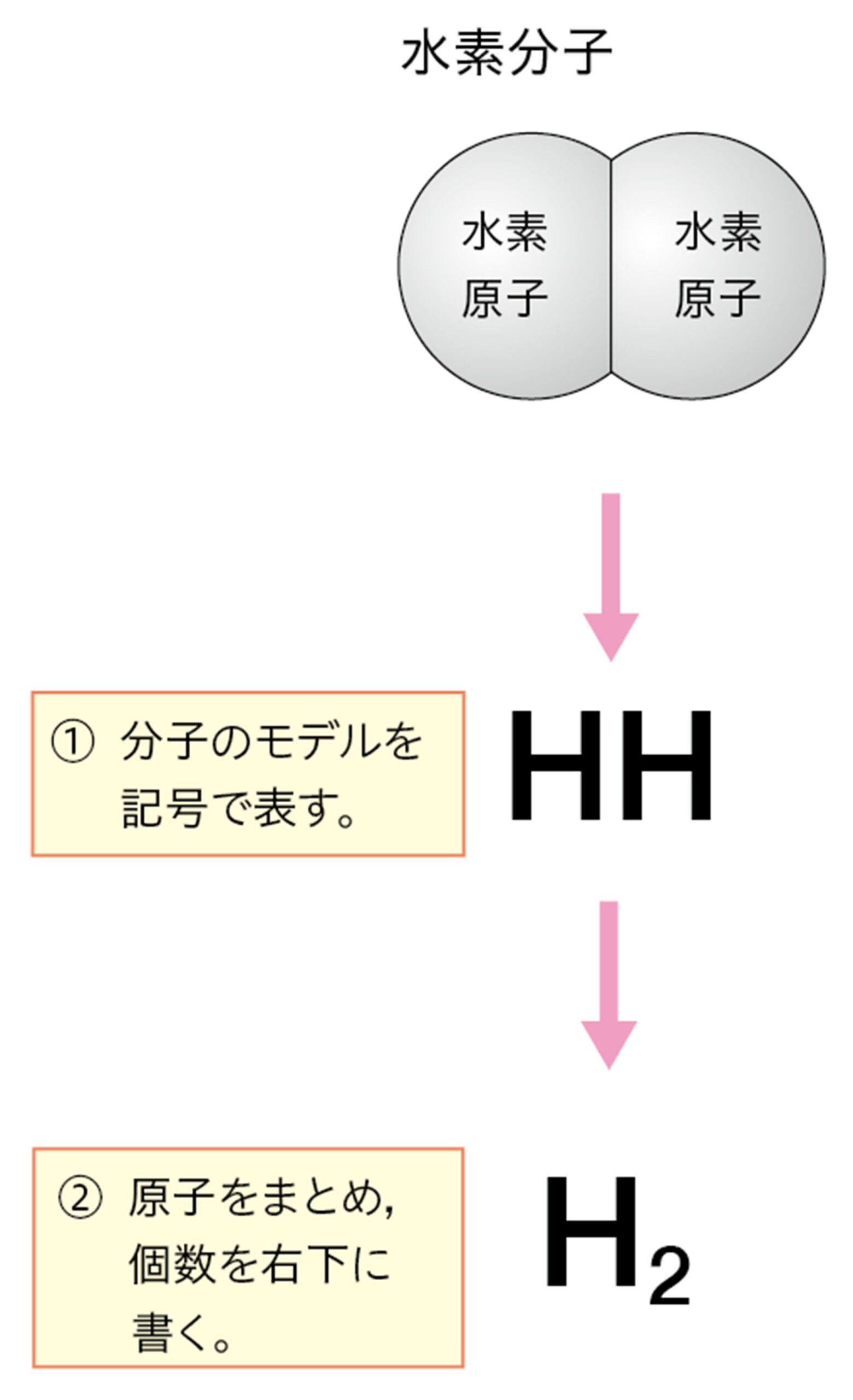
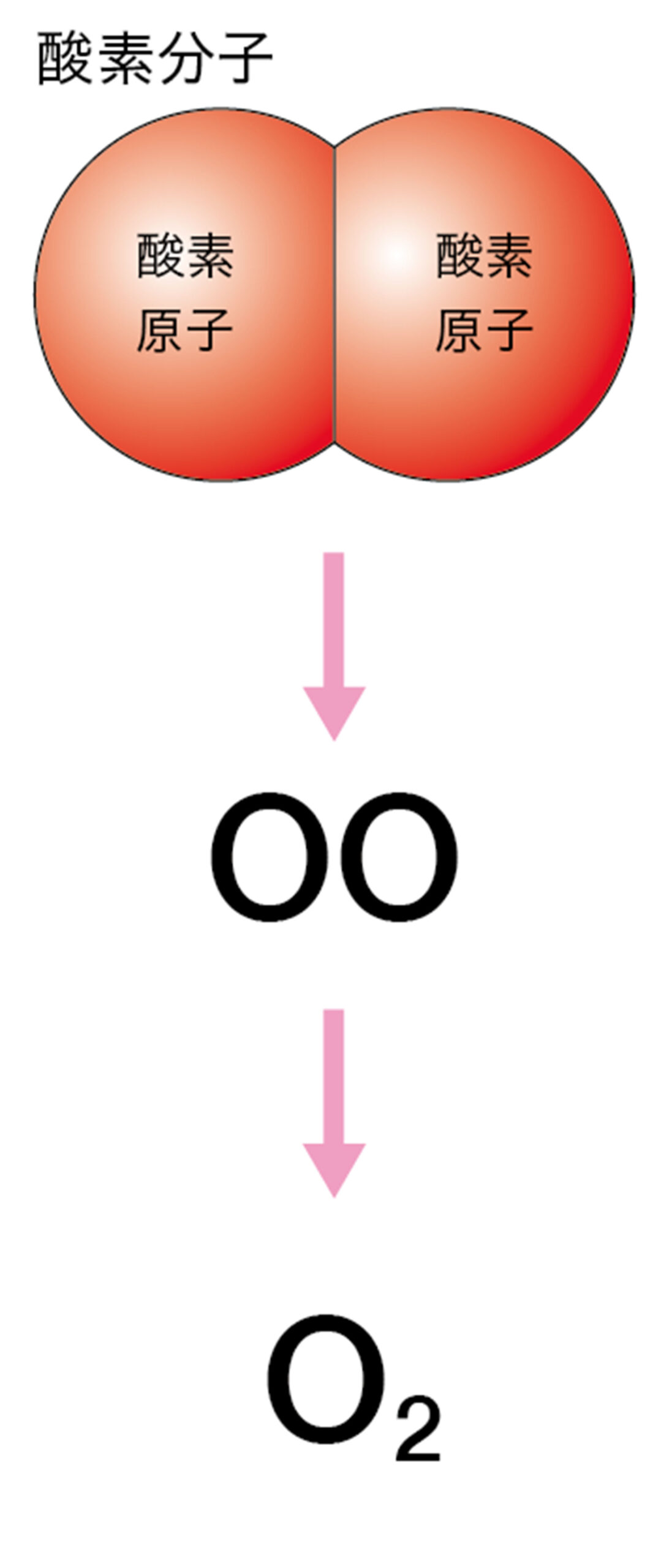
10 化学式
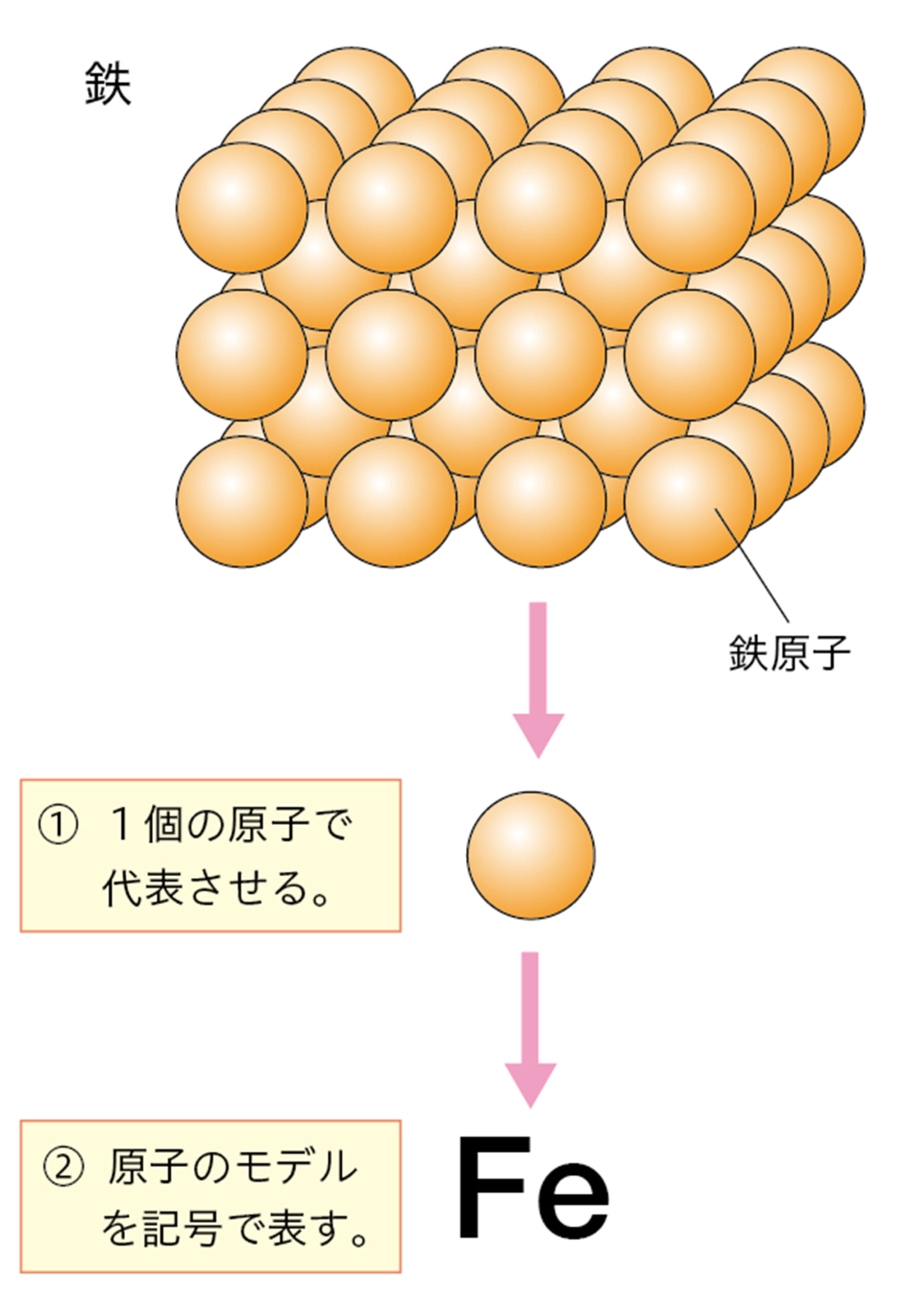
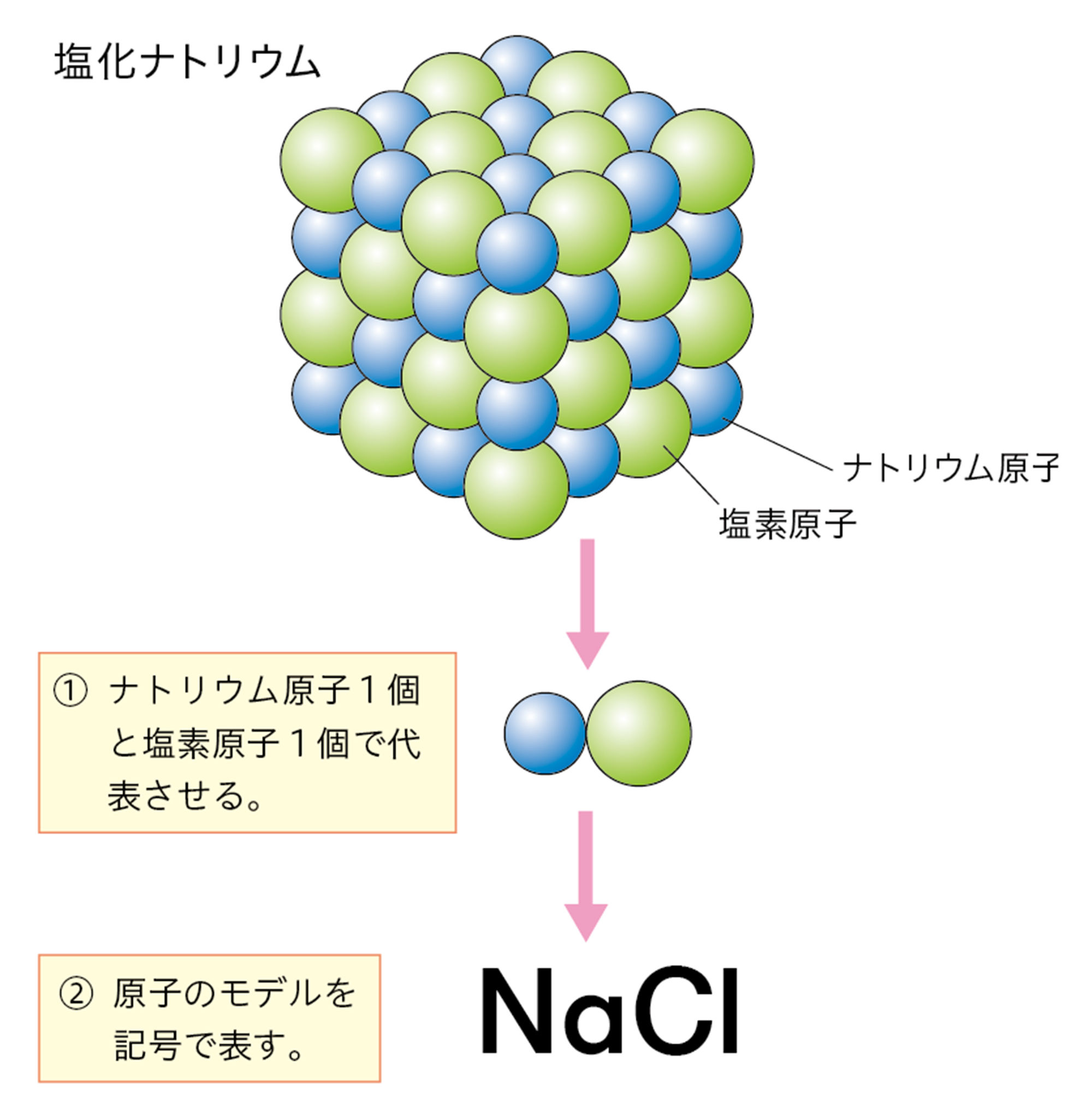
すべての物質は,元素記号を使って表すことができる。元素記号を使って表した物質の記号を【化学式】という。
単体や化合物には,それぞれ分子をつくる物質と,分子をつくらない物質がある。これらの物質は,化学式で次ページのように表される。
発展
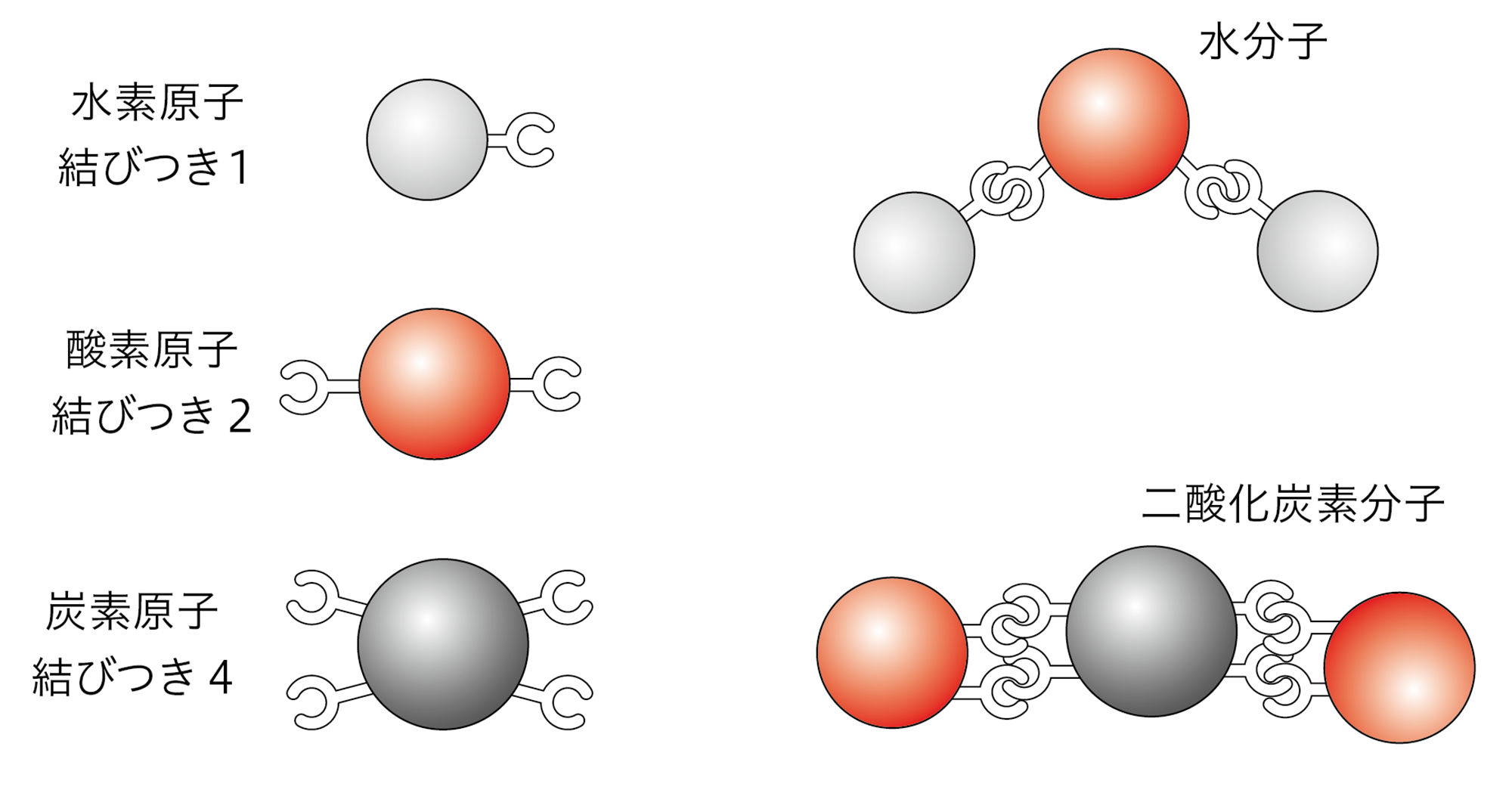
水分子や二酸化炭素分子などの化学式が決まっているのは,原子の種類によって,ほかの原子との結びつきの数が決まっているためと考えることができる。水素原子の結びつきの数は1,酸素は2,炭素は4として,その数を余らせないようにほかの原子と結びつくと,水分子や二酸化炭素分子ができあがる。
※このウェブページは中学校理科2年の学習内容です。<2年p.25>
● 分子をつくる物質の化学式
● 分子をつくらない物質の化学式
※このウェブページは中学校理科2年の学習内容です。<2年p.26>
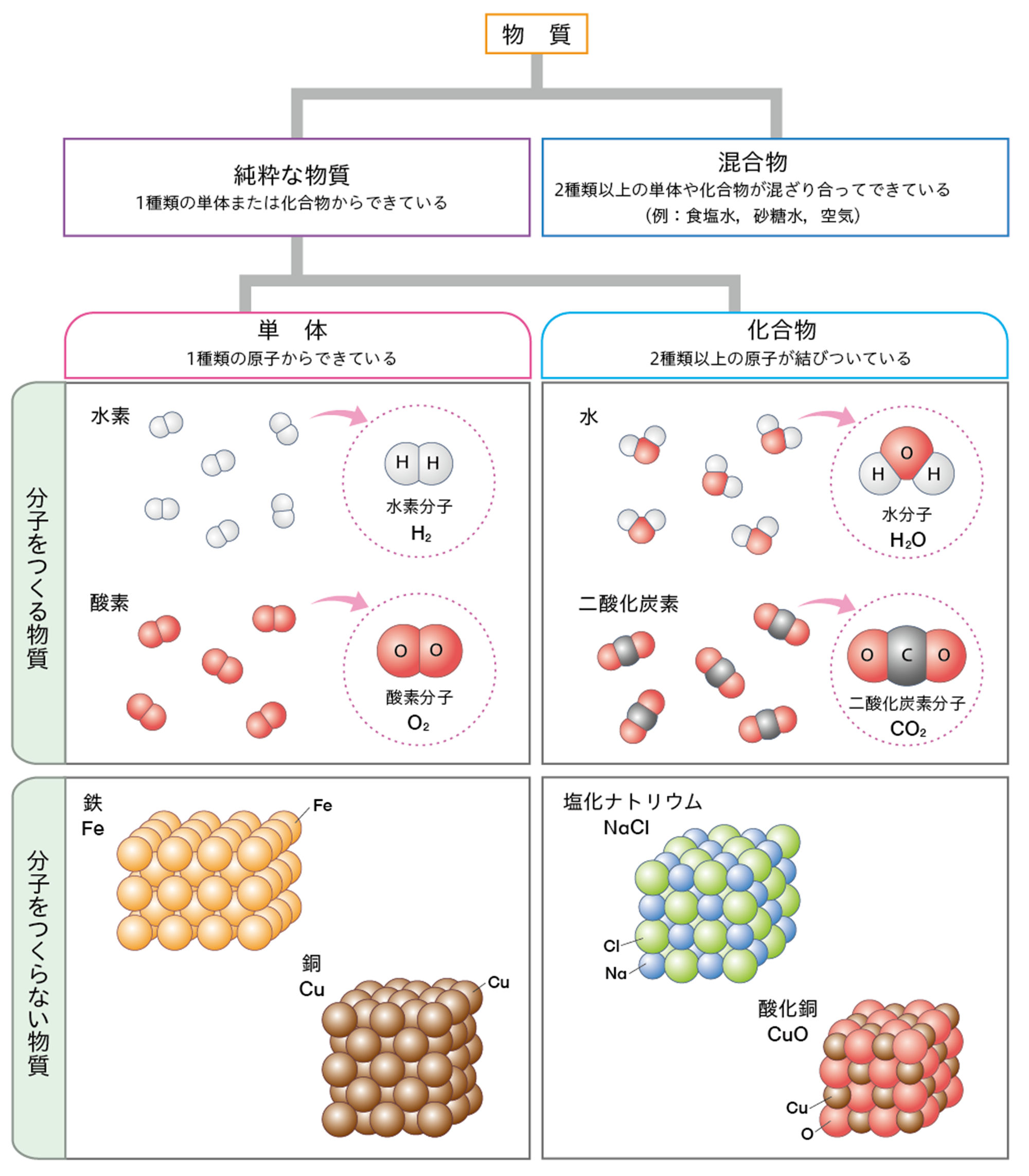
11 物質の分類
物質には純粋な物質と混合物がある❶。純粋な物質は,さらに単体と化合物に分けることができる。また,単体と化合物には,分子をつくる物質と分子をつくらない物質がある。これらの関係は,図16のようになる。
ふりかえり
❶ 純粋な物質…1種類の物質からできている。
混合物…いくつかの物質が混ざり合っている。

1年生で学んできた物質の分類には,
・有機物・無機物
・金属・非金属
・純粋な物質・混合物
があったね。
2年生からは,純粋な物質がさらに
・単体・化合物
・分子をつくる物質・分子をつくらない物質
に分類できるということだね。
酸化銅の銅原子と酸素原子の数の比は1:1です。化学式は,銅の元素記号を先に書きましょう。

ニュース
- 『腐ったミカン』の輝き―SSH校の取り組みの結果 2026年2月23日本年度スーパーサイエンスハイスクール(SSH)に指定されている,長野県の諏訪清陵高校の生徒チームは,腐ったミカンに紫外線を当てると光る現象に着目し,信州大学の協力のもと,その原因となる脂溶性(油分に溶ける)蛍光物質のひとつを特定して,さらに,その物質の化学構造を明らかにしました。今回明らかになった脂溶性蛍光物質は,ポリメトキシフラボノイドとよばれるグループの化合物の一種であり,研究ではカラマンダリンという品種のミカンを腐らせ,果皮から抽出・分析を行いました。また,別の水溶性蛍光物質の構造も推定できており,今後この構造が確定されれば,ミカンにふくまれる水溶性化合物としては初めての知見となる可能性があります。今回の成果は日本農芸化学会で発表され,企業奨励賞を受賞しました。 この研究のきっかけは,腐ったミカンが紫外線で光るというネットニュースだったそうです。これを見た,光る物質に興味を持っていた生徒の一人が,SSH課題研究として同級生と『ミカン班』を結成し,調査を始めました。『ミカン班』のメンバーは,“新しいものを見つけたい,という思いが研究の原動力”と語り,将来は天然有機化合物の研究を志しているそうです。指導にあたった教諭は,“これまでのスキルの積み重ねの結果”と評価しています。 箱の中に腐ったミカンが1つでもあると,まわりのミカンも腐らせてしまうから,しっかり取り除かなければならない―。こんな言い回しが流行した時代もありましたが,実は腐ったミカンこそ確かな輝きを放っていたようです。 もと記事リンク(外部サイトに繋がります。公開から時間がたつと繋がらない場合があります)
- あの信長も絶賛!『天下の名香』はどんな香り? 2026年1月7日「香木」とよばれる木の種類を知っているでしょうか?香木は生物学的な分類群ではありませんが,ビャクダン,ジンコウ,キャラといった,よい香りを放つ木を指すグループ名です。現在でもお香,フレグランスとして親しまれていますが,娯楽が少なかった古い時代には,その価値はさらに高かったことが知られています。 正倉院に収蔵されている香木「蘭奢待(ランジャタイ)」は,織田信長や足利義政など,歴代の権力者が求めた“天下の名香”として知られており,希少なものです。この“天下の名香”の正体とはいったい何なのか,宮内庁正倉院事務所は,専門家と協力して科学的な調査を行い,300種類以上の香り成分を検出しました。その中でも,ハチミツやシナモンのような甘い香りを持つ「ラブダナム」に似た成分が特徴的で,全体の香りに強く影響していることが明らかになりました。また,ランジャタイは東南アジア産のジンチョウゲのなかまの樹木であることがわかっていましたが,今回の調査によって,原木は8世紀後半~9世紀末に伐採された,または倒木したものである可能性が高いことが判明しました。 今回明らかになった,香りの成分と年代の測定は大きな成果ですが,研究チームはさらに,正倉院にどのような経緯でもたらされたのかを調べていきたいとしています。 もと記事リンク① もと記事リンク②(いずれも外部サイトに繋がります。公開から時間がたつと繋がらない場合があります)
- 1600年さびない鉄柱 2025年10月8日金属の「さび」は,教科書にも掲載されている,おだやかに進行する酸化現象のひとつです(2学年p.15)。さびが進行すると,もともとの金属とは異なる酸化物ができるため,変色したりもろくなったりしてしまいますが,世界にはなんと約1600年もの間,さびに耐えている鉄柱があるというから驚きです。 インドのニューデリーにあるクトゥブ・ミナール遺跡群には,高さ7.2m,重さ6トンの大きな鉄柱が立てられています。この鉄柱の起源は5世紀にまでさかのぼるとされていますが,特筆すべきは,屋外で風雨にさらされながら,建築当初から鉄柱としての原型を保ち続けていることです。 この耐久性の謎は,古くから科学者の関心を集めてきており,研究は1912年から始められていましたが,結論が出たのは100年近く経過してからの2003年となりました。インド工科大学の研究者らの発表によると,製鉄のなかでもさびにくい性質をもつ錬鉄(れんてつ:炭素をあまりふくまない鉄)を素材としており,加えて,一般的な鉄と比較すると,リンを多くふくむ一方で,硫黄とマグネシウムが少ないことがわかりました。リンが多くふくまれる金属は,さびに強くなることが知られています。また,「鍛接(たんせつ)」とよばれる,現代ではめずらしい技法が使われていることも判明しました。この技法は,金属どうしをとかさずに,固体のまま加熱・加圧して接着するもので,この技法を使うことで,リンが多くふくまれたまま加工ができた点が指摘されています。さらに,柱の表面には,鉄・酸素・水素で形成された化合物のうすい層ができており,この層がさびへの耐久性をさらに高めたことも考察されています。 当然,5世紀当時にはこのような化学的な性質はまったくわかっていなかったのですが,経験をもとに職人たちがこのような人工物をつくり上げたことは本当に圧巻です。その創意工夫に敬意を表して,研究チームではこの柱を“古代インドの冶金※技術の生きた証し”と表現しています。 ※冶金(やきん)…金属を鉱石などから取り出し,精製・加工して,実用可能な金属材料をつくり上げること。 もと記事リンク(外部サイトに繋がります。公開から時間がたつと繋がらない場合があります)
- 極限まで薄い金箔を作る 2025年7月23日「金箔」は,料理をゴージャスに見せる目的のためや,仏像や工芸品の装飾用として使われます。この金箔は,実は想像以上に薄く,一般にその厚さは0.0001mmほどです。ただそれでも,これは金原子500個分程度の厚さとなります。この金箔を,金原子1個分の厚さで作り出す試みに,スウェーデンのリンショーピング大学に所属する柏屋駿氏らの研究チームが成功しました。今回完成した,原子1個分の厚さしかない極限まで薄い金シートは,「Goldene」と名づけられました。 金箔を原子1個分の厚さにできると,どんないいことがあるのでしょうか?わかりやすいメリットは,貴重な元素である金を節約できるということです。また,炭素の研究から判明した現象なのですが,物質はその厚さが原子1個分になると,無数の原子が集まっている通常の状態と比べ,電気伝導性が飛躍的に高まるなど,異なる化学的性質を示すことがあり,この性質を利用できる可能性があることもメリットといえます。この,原子1個分の厚さしかない状態のシート状の物質は,特に2次元物質ともよばれます。 Goldeneを作るにあたっては,あつかいの難しい金の層を傷つけずに分離する方法が焦点となりました。この分離の操作には,1918年に東北大学の村上武次郎氏が開発した「村上試薬」が活用されたことも,注目すべき点といえるでしょう。 Goldeneには水素を生成する触媒としての有用な可能性が示唆されており,今後はその特性を活かした応用が期待されます。 もと記事リンク(外部サイトに繋がります。公開から時間がたつと繋がらない場合があります) 論文リンク
- 【宇宙ステーションで微生物によるバナジウム抽出に成功】 2023年3月1日バナジウム(原子番号23,元素記号V)は,建材や工具などに使用される鉄鋼を製造する際,強度を増すために添加されるなど,さまざまな形で私たちの生活に必要な元素です。 このバナジウムを,国際宇宙ステーション(ISS)の無重力条件下で,微生物の力を使って抽出することに成功したと,このたびNASAが発表しました。 生物を使って自然界に存在する金属元素を効率よく抽出する技術は「バイオマイニング」と呼ばれており,特に微生物を利用したものが宇宙空間で成功したことで,いつか人類が地球以外の星に進出したとき,現地で必要な金属資源を入手する技術として期待されています。 もと記事リンク プレスリリース
- 【緒方洪庵が遺した “開かずの薬瓶” 非破壊で内容物を解明:大阪大学 ほか】 2023年3月1日江戸時代末期の医師・緒方洪庵の遺した薬箱の中身が,最新技術で特定されました。 洪庵が晩年期に使用していた薬箱には,ガラス瓶に入った製剤22本などが入っていましたが,何本かは開栓不可能で,これまで中身が謎とされてきました。 今回,ミュオンビームを用いた元素分析法によって,白色の粉末が入った瓶の1本を非破壊で分析したところ,水銀,塩素のシグナルが観測され,瓶の表記の薬史学的な考証結果とあわせ,当時「甘汞(かんこう)」と呼ばれていた塩化水銀(I)であることが判明しました。 もと記事リンク
- 【太古の生物はどのように「増殖する」能力を獲得したのか? 100年の謎を実験で解明】 2023年3月1日太古の地球上で小さな分子が集まって複雑な大きな分子ができ,やがてそれらが増殖する分子集合体になって生命が誕生したという仮説があります。 これまで,大きな分子や分子集合体ができる様子がさまざまな研究において観察されていましたが,「増殖する」という生物の能力がどのように獲得されたかはわかっておらず,100年あまりの間,化学進化における「化学と生物学のミッシングリンク」となっていました。 今回,ペプチドを含むコアセルベートの液滴が小分子をエサとして取り込みながら成長し,外部からの刺激で分裂して増殖する様子が初めて観察されました。生命誕生の謎に迫るだけでなく,ペプチド複合体材料の生産技術にも活用されることが期待されています。 もと記事リンク 論文
- 【「ロウソクが燃えているとき,何が起きているのか」聞き手のワクワクを引き出す説明,できますか?】 2023年3月1日理科でとても有名な本を,新しい視点で。 理科の実験でもよく登場する「ロウソク」。ロウソクはなぜ燃えるのか? そして,ロウソクが燃えているとき,何が起こっているのか? ごく身近な現象ですが,そこには科学のタネぎっしり詰まっています。 この本は,化学や物理学での業績を数多くあげたマイケル・ファラデーの講演の記録です。ロウソクをはじめとした身近なものを使ったさまざまな実験から,ワクワクするような科学のエッセンスを引き出します。リチウムイオン電池の発明者で,2019年のノーベル化学賞受賞者でもある吉野彰さんが科学に興味をもつきっかけともなった一冊です。 『「ロウソクの科学」が教えてくれること 炎の輝きから科学の真髄に迫る、名講演と実験を図説で』 マイケル・ファラデー 著,白川英樹 監修,尾嶋好美 翻訳 SBクリエイティブ 2018年12月 ¥1,100(税込) ISBN:978-4-7973-9748-2 もと記事リンク