※このウェブページは中学校理科3年の学習内容です。<3年p.118>
1|電解質
1 原子の構造
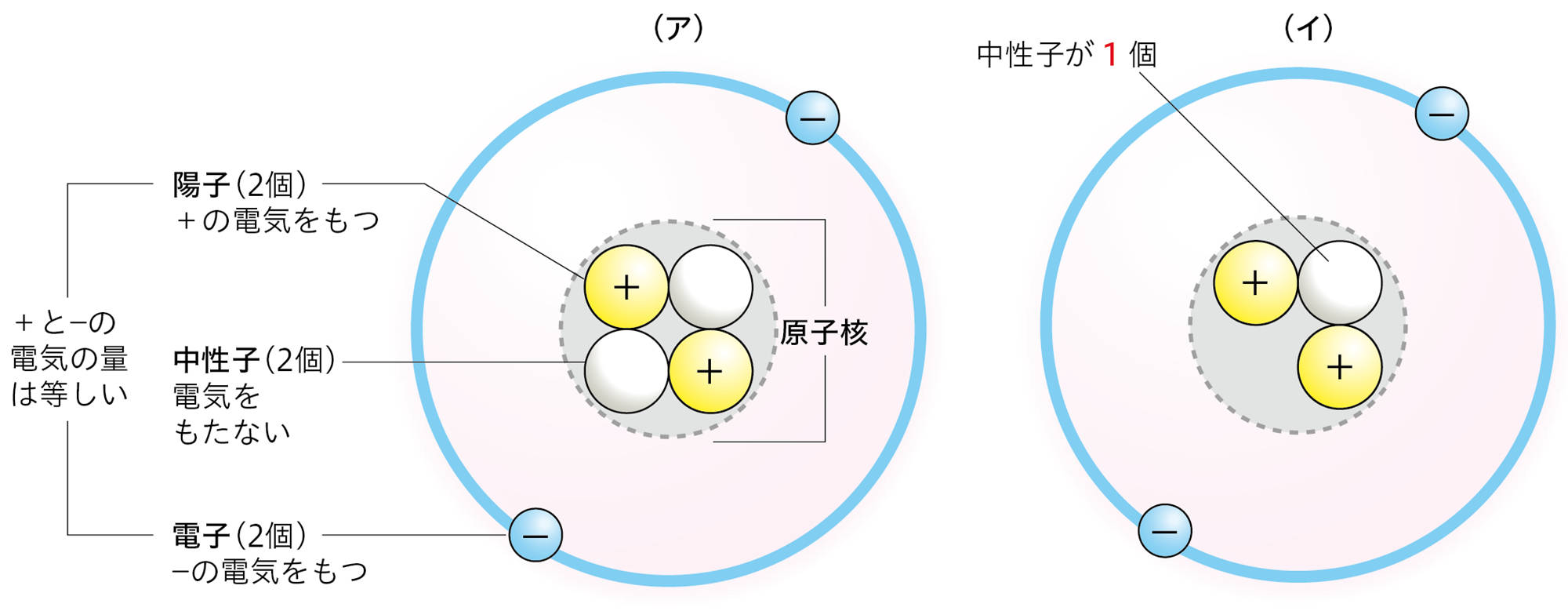
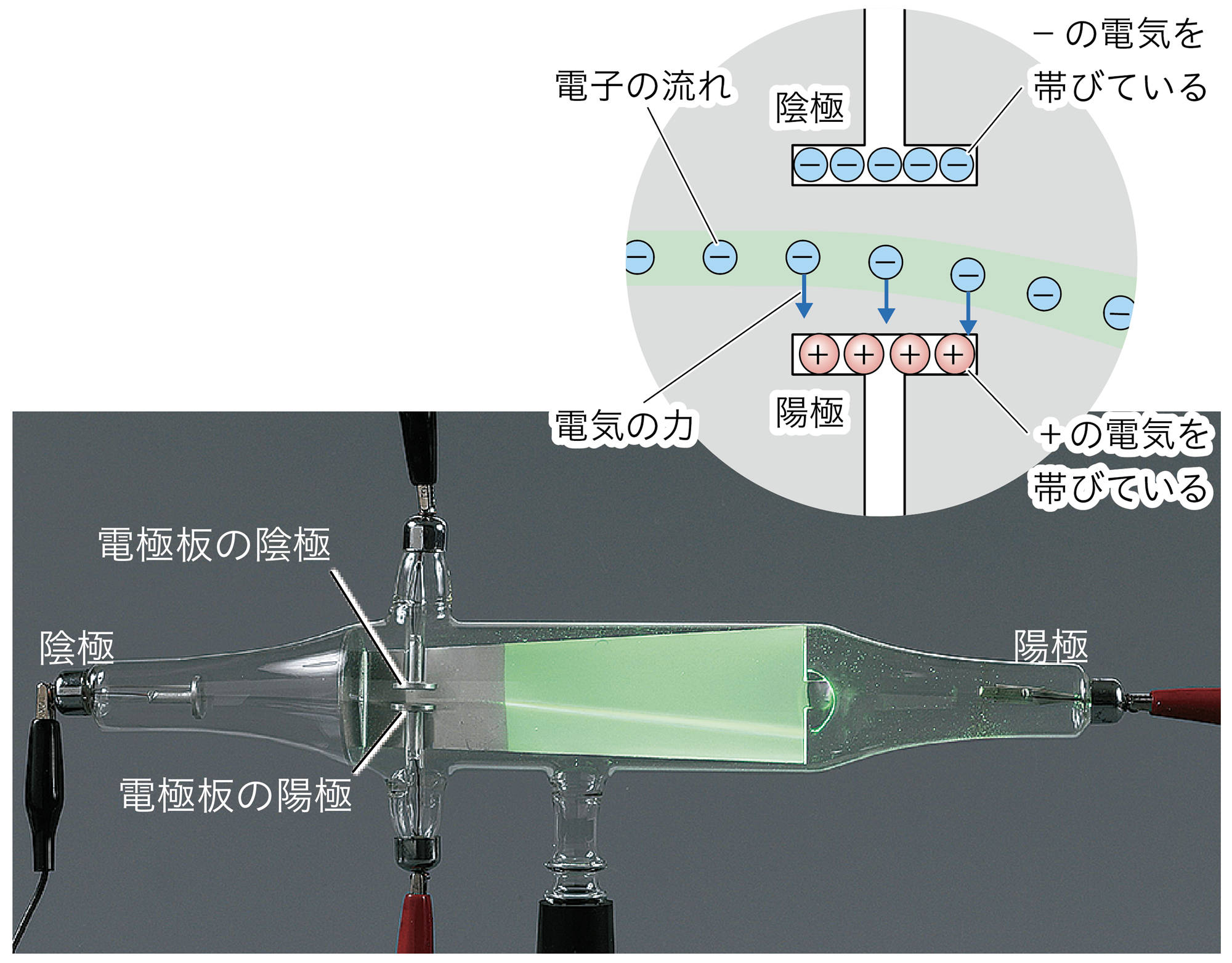
原子は,図1(ア)のように+の電気をもつ原子核と,− の電気をもつ電子からできている❶。原子核は,原子の中心にあり,そのまわりに電子が存在する。また,原子核は,+の電気をもつ陽子と,電気をもたない中性子が集まってできている。
陽子1個がもっている+の電気の量と,電子1個がもっている − の電気の量は等しい。原子の中の陽子の数と電子の数が等しいので,原子全体としては陽子と電子がたがいの電気を打ち消し合い,電気を帯びていない状態になっている。
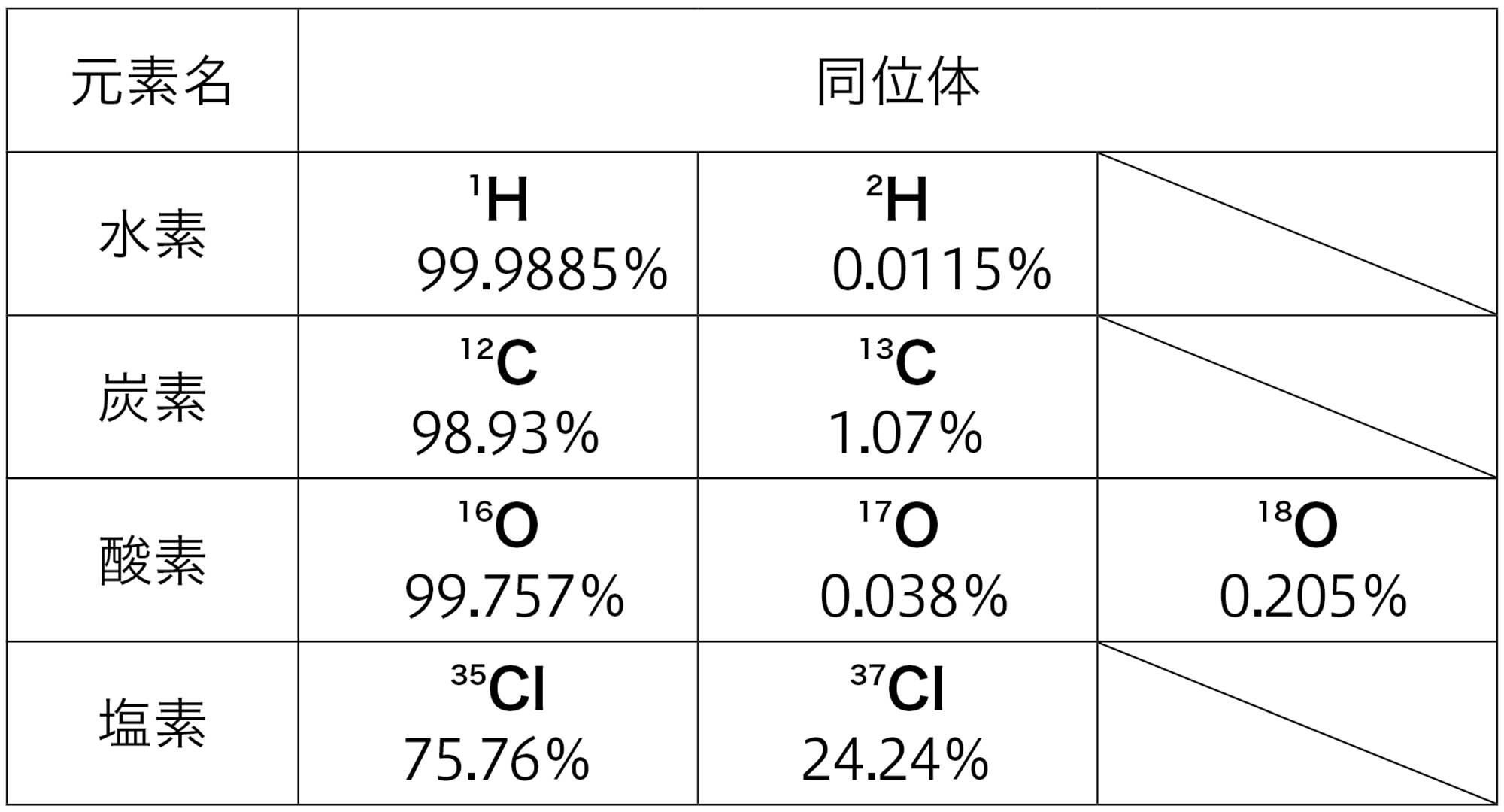
また,同じ元素であっても,原子によっては中性子の数が異なることがある(図1(ア)(イ))。このような原子どうしを同位体という。原子核の陽子の数が同じであれば,原子の性質はほぼ同じである。
2年生で学習した「元素」とは,同位体をまとめてよぶときの用語です。元素の化学的性質は陽子の数にもとづいて決まります。

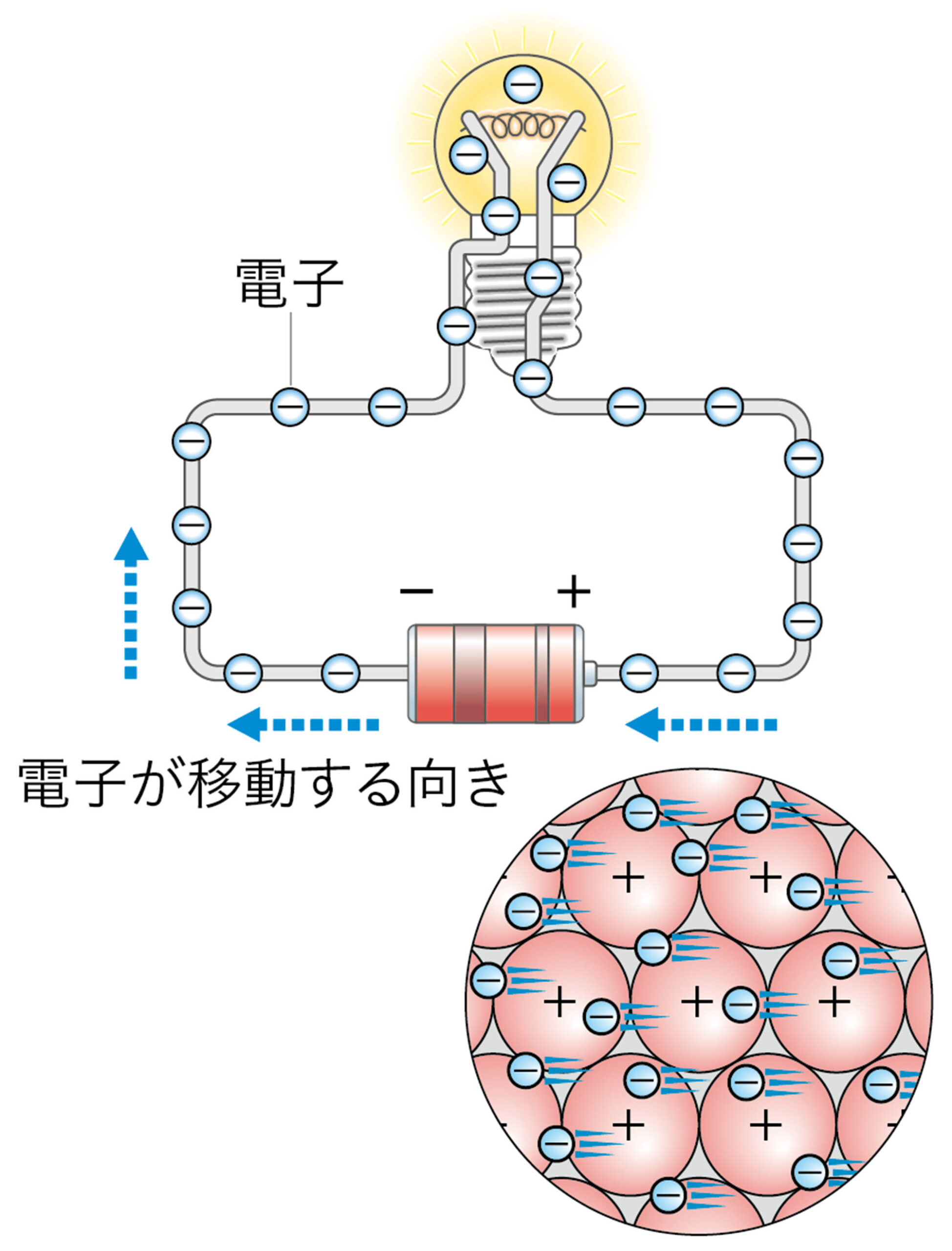
❶ 静電気は物質の間を電子が移動することによって起こる。また,導線の中には自由に動ける電子があり,これが電流の正体である。このような現象が起こるのは,原子が電子をもっているからである。
❷ 出典:NIST Physical Measurement Laboratory
※このウェブページは中学校理科3年の学習内容です。<3年p.119>
図2のように,塩化ナトリウム水溶液には電流が流れる。この現象を,原子のモデルを用いて,どのように科学的に探究できるだろうか。
探究1 電流が流れる水溶液

電源装置につないだ電極を蒸留水に入れても,電流は流れません。同じように,固体の塩化ナトリウムも電流が流れません。しかし,塩化ナトリウム水溶液には電流が流れます。これはどのようなしくみでしょうか?
図2 物質に電流が流れるか調べる実験
電流が流れる水溶液には,何が関わっているか。原子や電子のモデルで説明する。

「物質が水に溶ける」とは,物質をつくっている粒子がばらばらになることだったね。
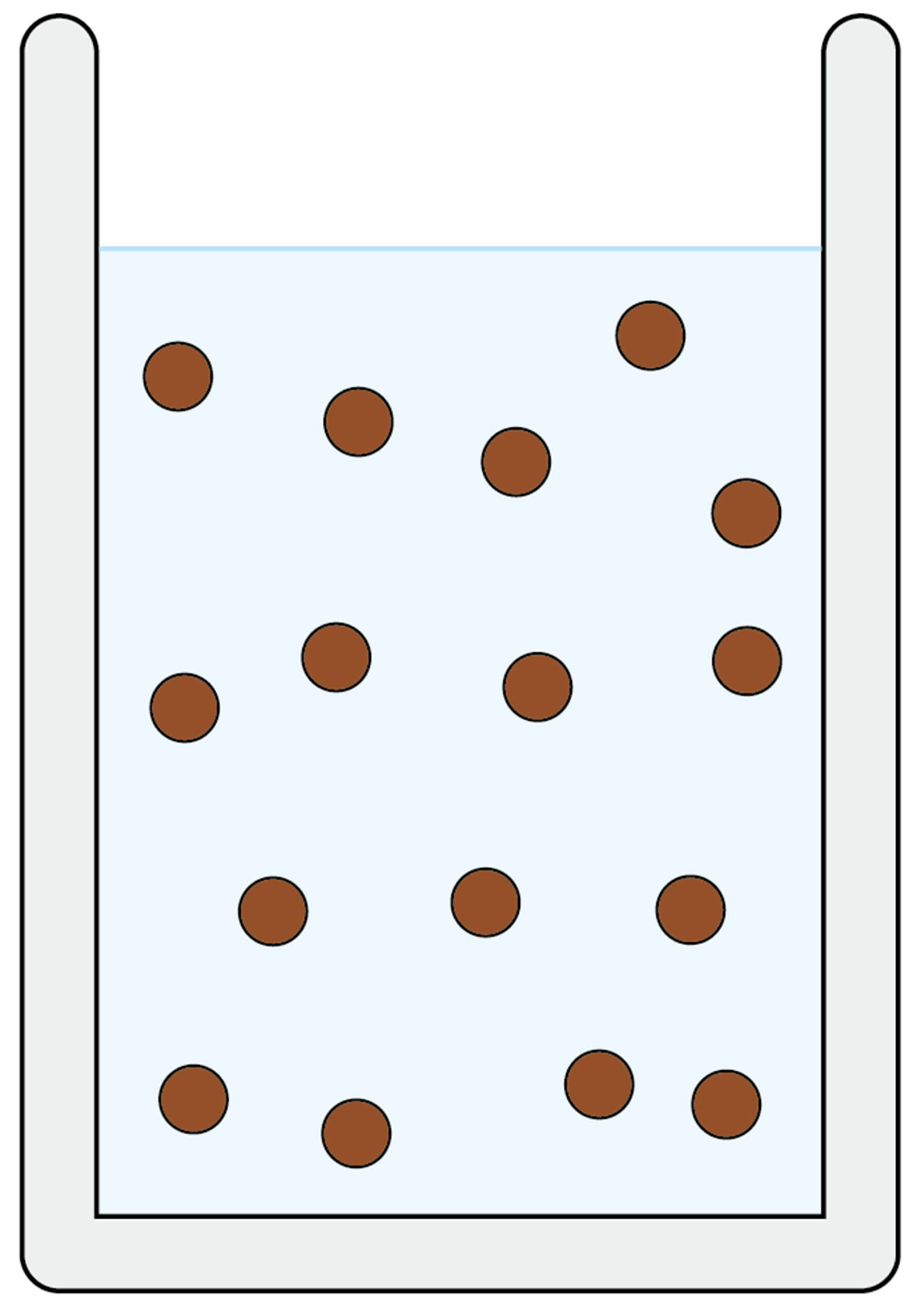

回路には電流が流れるね。水溶液の中でも電流が流れるとはどういうことだろう。

電源装置が必要だね。電流の大きさもはかりたいな。
水に溶ける物質を集めて試してみよう。


電気が流れたとき,水溶液にはどんな変化が見られるかな。
※このウェブページは中学校理科3年の学習内容です。<3年p.120>
準備
塩化ナトリウム水溶液(5%),砂糖水(5%),塩化銅水溶液(5%),塩酸(5%),水酸化ナトリウム水溶液(5%),エタノール水溶液(5%),蒸留水,50cm³ビーカー(8),電極,電流計,電源装置,豆電球,クリップつき導線,洗浄びん,保護めがね
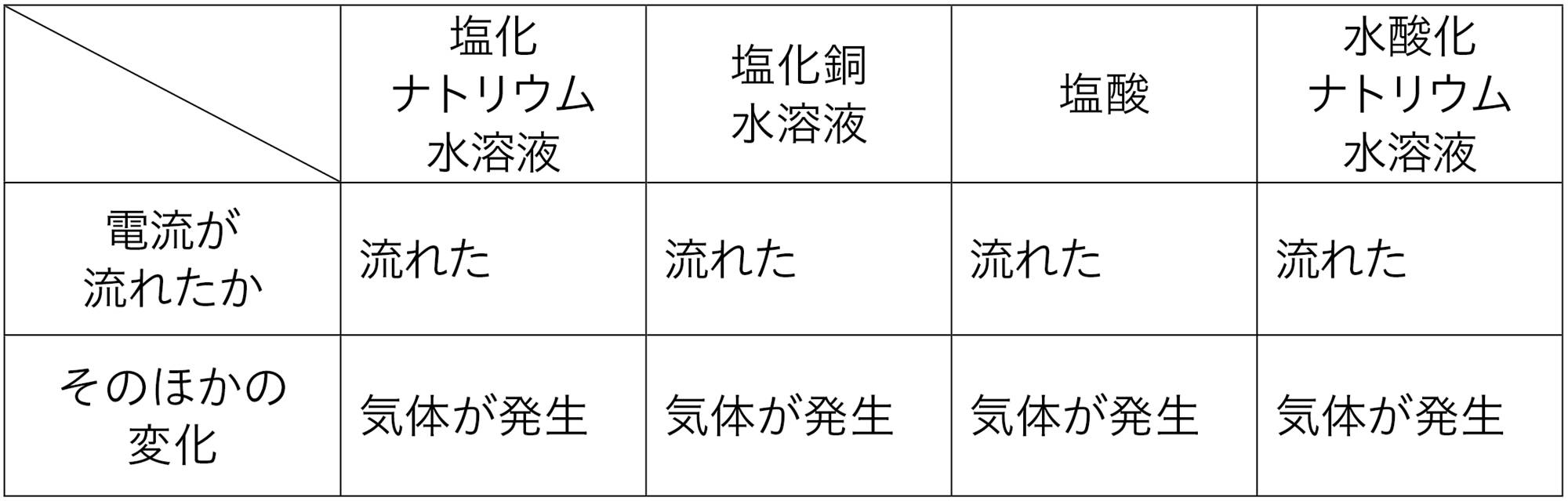
各班であつかう水溶液を分担する。それぞれの水溶液や蒸留水に電極を入れて,3〜6Vの電圧を加え,水溶液に電流が流れるか調べる。
注意!! 酸性やアルカリ性の水溶液は,目に入ると危険なので,保護めがねをかける。手に触れたりしたら,すぐに大量の水で洗う。換気をよくして実験を行い,発生する気体を吸いこまない。
図3 探究1の結果例
- 水溶液に電流が流れるということは,電子が流れているのだと思う。
- 2年生の静電気の実験で,電子だけが移動することを学習した。これをもとにすると,溶質から電子が出て水の中に広がったという考えはありえる。
- 電流が流れる水溶液では電極で化学変化が起こっているようだ。
電子は原子から出たのかな。電子が出た原子はどうなるのかな?

物質は水に溶けると,電子を出すようになるのかな?


2 年生で,原子は「化学変化によって,それ以上分けられない」と学びました。これは,かつて原子という考えが広まったときの決まりです。しかし, その後研究が進み, 今では原子がp.118図1 のような3 種類の粒子からできていることが知られています。
※このウェブページは中学校理科3年の学習内容です。<3年p.121>
2 電解質と非電解質
塩化水素や塩化ナトリウム,塩化銅などは水に溶け,その水溶液には電流が流れる。一方,砂糖やエタノールなどは水に溶けるが電流は流れない。水に溶けたときに電流が流れる物質を電解質といい❶,水に溶けたときに電流が流れない物質を非電解質という。
電解質を溶かした水溶液に電流を流したときの電極の変化について,どのように科学的に探求できるだろうか。
探究2 塩化銅水溶液の電気分解

探究1で塩化銅水溶液に電流を流したとき,電極のまわりが黄色くなったり,気体が発生したりしたよ。これは何が起こっているんだろう。
2年生で水の電気分解を行いましたね。図3(b)も電気分解の一種です。また,塩化銅の化学式はCuCl₂です。これをもとに考えてみましょう。

塩化銅水溶液を電気分解しているとき,水溶液の中では何が起きているか。電極に現れる物質から考える。

水の電気分解では,陽極からは酸素,陰極から水素が発生したよ。塩化銅水溶液も何かに分解されるのかな。
電極は電気を帯びているんだよね。どちらが+で,どちらがーだったかな。


電極を入れかえたら,発生する物質も入れかわりそう。これを,原子が帯びている電気で説明できないかな。

まずは探究1と同じように,電気分解を行えばよいね。
発生する気体の予想をもとに,安全に気をつけて実験しよう。


電極から現れる物質を確認する方法を思い出そう。
❶ ぬれた手で電化製品にさわると感電する危険があるのは,手の汗や水道水にも電解質がふくまれているからである。
※このウェブページは中学校理科3年の学習内容です。<3年p.122>
準備
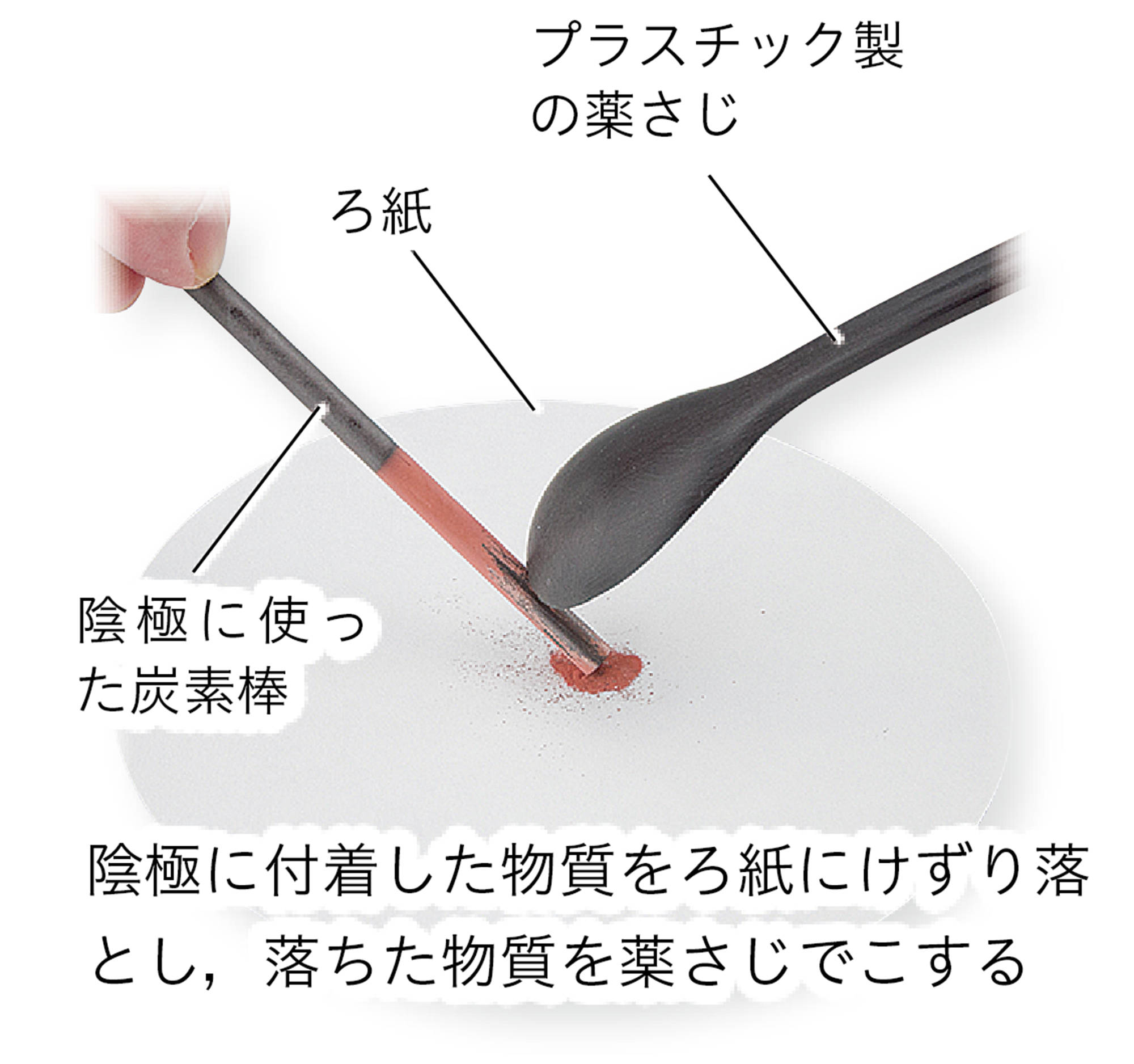
塩化銅水溶液(5%)❶,炭素棒電極(またはえんぴつのしん),発泡ポリスチレンの板,100cm³ビーカー,電流計,電源装置,クリップつき導線,スポイト,ペトリ皿,薬さじ(プラスチック製),ろ紙,赤インク,保護めがね
電気分解のとき,電源装置の+極につないだ電極を「陽極」,−極につないだ電極を「陰極」といいます。炭素棒やえんぴつのしんは導体で,ここでは電極として使用します。

1.塩化銅水溶液に電流を流す
図のように実験装置を組み立てて,0.5Aの電流を流す。
電流を流しているときの陰極や陽極のようすを観察する。
注意!! 換気をよくして実験を行う。
2.電極に発生する物質を調べる
陰極に付着した物質や,陽極付近の液の性質を調べる。
注意!! 直接,鼻を近づけてにおいをかがない。手であおぎよせるようにしてかぐ。
❶ 質量パーセント濃度
※このウェブページは中学校理科3年の学習内容です。<3年p.123>
注意!! 実験後の塩化銅水溶液の処理は,先生の指示にしたがう。
ポイント
- 陰極,陽極で生じた物質には,どのような性質があるか。
- 陰極,陽極をつなぎかえたときに,どのような変化が起こったか。
ポイント
- 陰極,陽極と生じる物質にはどのような関係があるか。
- 原子のモデルで水溶液の中のようすを考える。
電極で電子の移動する向きを考えよう。その向きは電流の流れと逆だよね。−の電気を帯びているのは陽極だろうか,陰極だろうか。

※このウェブページは中学校理科3年の学習内容です。<3年p.124>
探究2 結果から考察する
図5 探究2の結果例
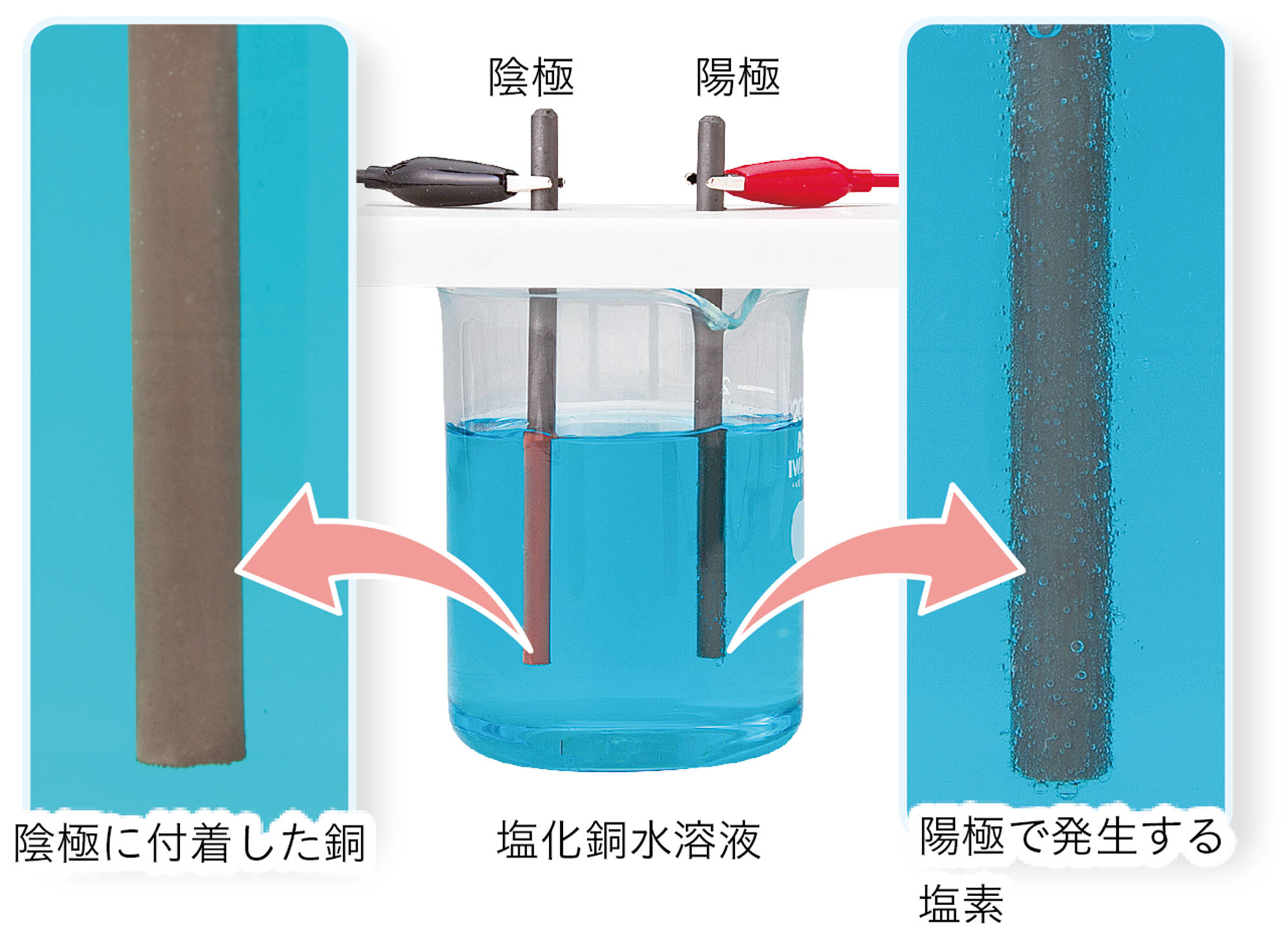
- 陰極に付着した物質は,赤色で金属光こう沢たくがあることから銅であることがわかる。
- 陽極で発生した気体は,特有の刺激臭があることや,赤インクの色が消えたことから塩素であることがわかる。
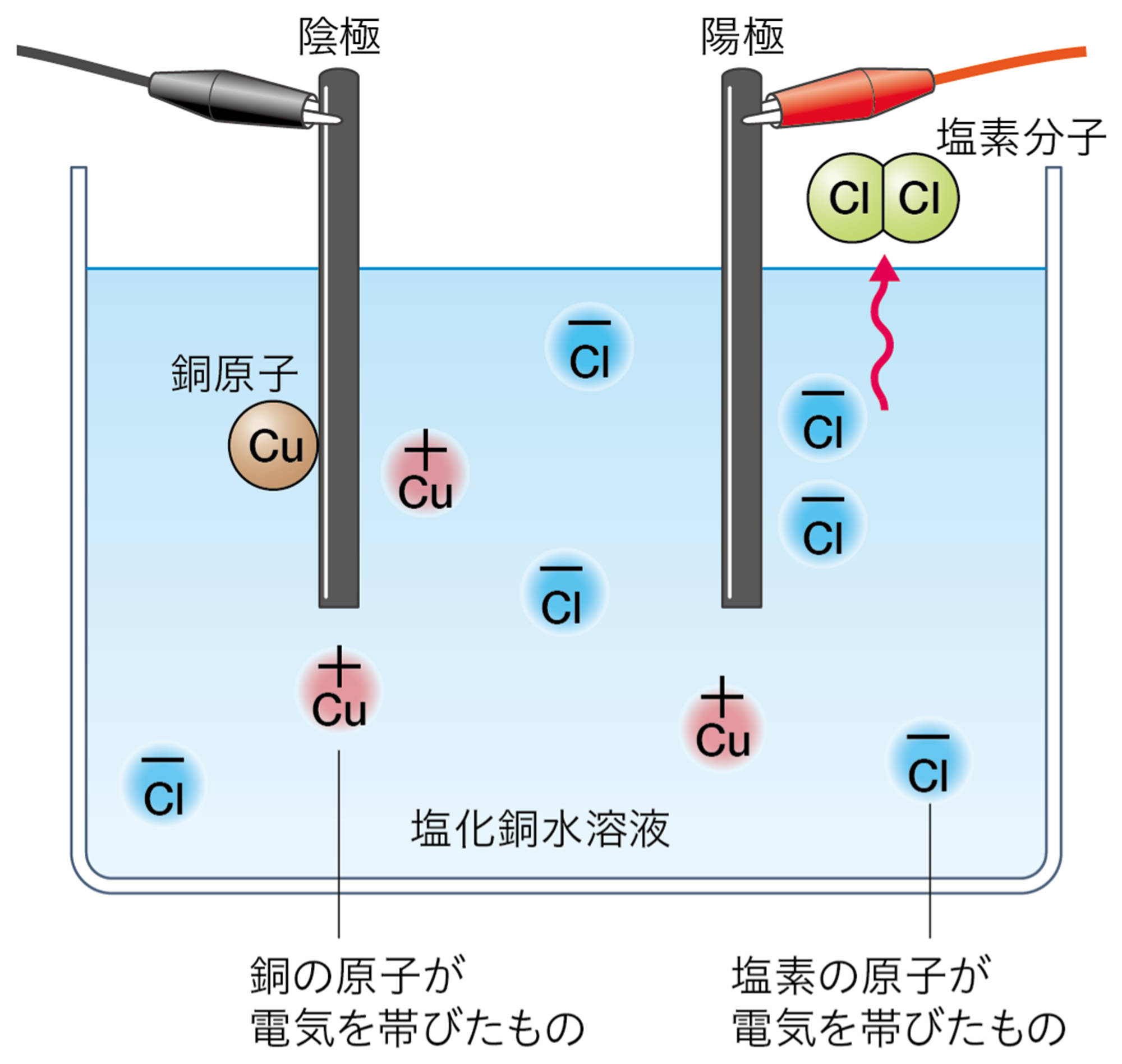
- 銅は陰極から現れることから,水溶液中で,銅の原子が+の電気を帯びたものに変化しているのではないか。
- 塩素は陽極から現れることから,水溶液中で,塩素の原子が − の電気を帯びたものに変化しているのではないか。
※このウェブページは中学校理科3年の学習内容です。<3年p.125>
3 電気泳動
探究2のように,電解質の水溶液に電圧をかけて電解質を分解する方法を電気分解という。また,図8のように,水溶液中の物質が電圧をかけたときに移動する現象を電気泳動という。
探究2の電気分解では,陰極側に塩化銅水溶液中の銅が引きつけられ,陽極側に塩素が引きつけられている。このことから,水溶液中の銅は+の電気を帯びており,塩素は−の電気を帯びていることがわかる。また,図8の電気泳動では,青色のしみ(+ の電気を帯びた銅)が陰極側に動くので,水溶液中に+の電気を帯びた粒子があることがわかる。
このように原子が電気を帯びたものをイオンという。
電気を帯びた塩素原子は色を示さないので図8の実験では確かめられませんが,陽極側へ動いています。

図8 塩化銅水溶液の電気泳動
ニュース
- 中性子の数は何個がよい?原子核の不安定さの研究 2026年3月1日3学年の教科書p.118では,ヘリウム原子の構造が紹介されています。この図1では,原子番号2番のヘリウム原子は,二つの陽子をもっており,二つの中性子をもつものが大半を占めることが説明されています。このように中性子が二つの場合と,あるいは四つの場合に,原子の状態は比較的安定することは研究が進んできていましたが,たとえば,中性子の数が三つの場合,二つの場合よりもどれほど不安定になるかは,くわしくわかっていませんでした。 東北大学などの研究グループは,三個の中性子のみ、三個の陽子のみから成る量子系を実験的につくり出し,その不安定性を明らかにしました。三中性子系は,二中性子系や四中性子系と異なり,不安定であることが判明しました。また三陽子系は,不安定ながらも,三中性子系と類似した特徴をもつことも明らかとなりました。 これらの成果は,原子核を構成する粒子どうしの間にはたらく力の理解や,寿命を迎えた恒星が変化して生じる,中性子を主成分とする天体である中性子星の構造解明に貢献するものであり,今後の原子核の研究や宇宙物理学の発展に重要な示唆を与えるものです。 もと記事リンク(外部サイトに繋がります。公開から時間がたつと繋がらない場合があります)
- 過去最高,超エネルギーのニュートリノが検出 2025年12月10日「ニュートリノ」という物質の名前を聞いたことがあるでしょうか。この物質は,電気的に中性な素粒子(原子核をつくる,きわめて小さな粒子)で,他の物質とほとんど反応しない性質をもつため,なんと地球さえも簡単に通り抜けてしまいます。この透過性のため,宇宙空間を移動して地球に到達したニュートリノからは,透過してきた他の天体についてなど,さまざまな情報が得られることが期待されています。ニュートリノの観測では,日本にある施設「スーパーカミオカンデ」が大きな貢献を果たしていることも有名です。 このニュートリノについて,国際研究チームは,イタリア南部シチリア島近海の地中海深海に設置した検出器を用いて,2023年2月に過去最高のエネルギーをもつものを観測したと発表しました。検出されたニュートリノは,約22京※電子ボルトのエネルギーをもち,従来の観測値の約30倍に達しています。これは,銀河系の外から飛来した可能性が高いとされていますが,発生源や高エネルギーの生成メカニズムについてはまだ解明されていません。研究チームは,今後も継続的な観測を行っていく方針です。 ※1京:10 000 000 000 000 000 1億の1億倍に相当。 もと記事リンク(外部サイトに繋がります。公開から時間がたつと繋がらない場合があります)
- 現代の錬金術:鉛から金をつくる価値とは 2025年8月10日スイスのジュネーヴとフランスの国境部にまたがって位置する,世界最大規模の素粒子物理学研究所「欧州原子核研究機構」(通称CERN)で,“現代の錬金術”ともいえる研究成果が得られました。CERNにあるLHCとよばれる大型の加速器によって,鉛の原子どうしを光速に近い速度で,ごく近距離をすれちがわせることで,きわめて短時間,かつ,きわめて微量ですが,「金」の原子が生成されることが確認されたのです。 もともと,鉛の原子と金の原子では,陽子の数が鉛は82,金は79という差しかなく,この3つの陽子を失わせることで,理論的には鉛から金をつくり出すことも可能なことがわかっていました。しかし,原子から陽子をとるには非常に大きな力が必要で,これまで現実的には不可能とされてきました。これが,いわゆる“錬金術”が成立しない理由です。今回の実験結果は,それをくつがえす革新的な成果といえます。 今回,従来に比べ類をみない規模で鉛から金が生成したことが確認されていますが,それでも,2015〜2018年の実験で約860億個,質量にすると約29ピコグラムの金原子核という量であり,これは髪の毛1本300万分の1ほどにすぎません。仮に,1グラムの金を生成するとなると,今回の実験をもとに試算すると,次のようなコストがかかることにます。 ・必要なエネルギー量… 1.3×1026ジュール ・必要な電気代…日本円で30円/kWhとして,1京8000兆円 どちらもちょっと想像がつかない大きさです。イメージしやすい例にさらに換算すると,鉛から65グラムの金をつくるために,地球上のすべての海を沸騰させるだけのエネルギーが必要となり,また,そのためには日本の国家予算※1の10000倍以上の金額をつぎ込む必要が出てくるというスケールです。一方,ふつうの金は1グラムあたり15000~18000円程度※2で市場に流通していることから,とてもではないですが,現在の市場価値に影響を及ぼす可能性は考えられません。 しかしながら,今回,原子の種類が変わる現象が確認されたことは,理論モデルの精度向上や,加速器の建設に新たな知見をもたらす,科学全般に寄与する大きな成果であることは間違いありません。 ※1 2025年度予算をもとにしている。 ※2 2025年6月の国内金相場価格を参照。 論文リンク(外部サイトに繋がります。公開から時間がたつと繋がらない場合があります)
- 教科書も書き換わる?新たな化学結合「-電子結合」発見 2025年4月9日これまで,炭素原子どうしが結合する場合,2つの原子が価電子を出し合って共有電子対をつくることで共有結合が形成されることが広く知られていました。しかし,今回発表された東京大学と北海道大学による論文では,炭素原子間の新しい結合様式「-電子結合」が発見され,また,実験的に実証されました。この結合は,炭素どうしが電子1つだけを共有することで形成されるもので,従来の化学結合の理解を根本から覆す可能性があります。 この-電子結合を持つ化合物は,予想に反して非常に安定であり,結晶状態で100℃以上の高温や溶液中の大気下でも扱えることが判明しました。さらに,この結合は近赤外光を吸収する特性を持ち,有機材料の分子骨格を小型化する新しい材料開発への応用が期待されています。 実はこの結合様式は,理論的には約1世紀前に提唱されていたもので,今回の成果は,100年にも及ぶ化学者たちの挑戦に終止符を打つ,非常に重要で,化学結合の理解を深める画期的な一歩として位置付けられています。教科書の内容にも影響を与える可能性があるほど意義深いものです。 もと記事リンク(外部サイトに繋がります。公開から時間がたつと繋がらない場合があります) 論文リンク
- 【水と化学的に同じはずの「重水」は甘かった】 2023年3月1日原子核に中性子が1個多く含まれている重水素を含む「重水」は,水と同じH₂Oの化学式で表されます。重水も通常の水も化学的には全く同じ組成なので,同じ性質をもつはずです。しかし,重水を実際になめた人々からは「重水は甘く感じる」と言われていました。 本当に重水は甘いのかについて,今回実験が行われました。その結果,不思議なことに,マウスは重水の甘味を感じていないのに,人間にとって重水は「甘い」と感じられることが分かりました。 もと記事リンク 論文